서 론
리튬 주요 발생원과 수계 내 농도 분포
자연적 기원
인위적 기원
수생 동물 및 육상 식물에서의 생물학적 Li 축적 및 독성 영향
수생 동물에서의 Li 축적 및 독성 반응
육상 식물에서의 Li 축적 및 독성 반응
리튬의 생리·독성 반응에 대한 통합적 고찰
리튬 동위원소 분별 및 오염원 추적 사례
리튬 동위원소 분별의 주요 경로
수계 내 인위적 기원 Li 추적 사례
사용 후 LIB의 Li 원산지 추적 사례
인위적 Li 오염원의 δ7Li 조성 특성 비교
결 론
서 론
우수한 전기화학적 특성을 지닌 리튬(lithium, Li)은 이차전지 산업에서의 수요가 지속적으로 증가하고 있으며(Oruch et al., 2014; Swain et al., 2017; Ngoy et al., 2025), 전 세계 Li 자원의 상당량이 배터리 제조에 활용되고 있다(Kavanagh et al., 2017). 최근 수요 확대에 따라 Li의 연간 생산량은 2010년에서 2021년 사이 256% 증가하였으며 2041년경에는 약 700,000 Metric Ton 이상 생산될 것으로 예측된다(Adeel et al., 2023; Liu et al., 2023). 이에 따라 Li 자원의 활용 가속화에 따른 리튬이온전지(lithium-ion battery, LIB)의 생산 및 사용이 확대되고 사용 후 LIB의 발생량 또한 꾸준히 증가할 것으로 예상된다. 특히 LIB 재활용 공정에서 발생하는 폐수와 침출수는 Li을 수계와 토양으로 유입시키는 주요 배출원으로 작용할 수 있으며(Dobosy et al., 2023), 용존 형태의 Li은 환경에서 높은 이동성을 보이기 때문에 오염 확산 가능성이 크다. 이러한 Li 오염은 생물체 내 축적을 통해 생태계와 인체 건강에 잠재적인 위해를 유발할 수 있다는 점에서 보건학적 우려가 제기되고 있다(Bolan et al., 2021; Yang et al., 2024).
리튬의 환경 내 거동과 생태 독성에 관한 기존 연구는 주로 식물과 수생 생물을 대상으로 한 축적 특성과 반응 기작 규명에 집중되어 왔다(Aral and Vecchio-Sadus, 2008; Shahzad et al., 2016). Li은 생물체 내에서 알칼리 금속인 나트륨(sodium, Na), 칼륨(potassium, K)과 유사한 이온 반응성을 지니고 있어 세포막을 통한 흡수와 조직 간 이동과정에 쉽게 관여하며, 다양한 생물종에서의 축적 가능성을 높인다(Aral and Vecchio-Sadus, 2008). 식물 내 과도한 Li 축적은 엽록소 함량 감소와 광합성 효율 저하를 유발하고, 과도한 활성산소종(reactive oxygen species, ROS) 생성으로 인한 산화적 스트레스를 통해 세포 손상을 일으키는 것으로 보고되었다(Shakoor et al., 2023; Buendía-Valverde et al., 2024). 이러한 반응은 장기적으로 대사 경로의 교란과 생리적 이상을 초래하여 식물 생장을 저해할 수 있다. 수생 생물에 대한 실험적 연구에서도 Li 노출 농도에 따른 조직 내 축적 패턴, 산화적 스트레스 반응, 신경 생리적 변화 등이 확인되고 있으며(Yang et al., 2024), 특히 뿌리 조직이나 아가미와 같이 이온교환이 활발한 기관에서 선택적 축적이 일어나는 특성이 보고되었다(Thibon et al., 2021). 이러한 결과는 Li이 낮은 농도에서도 장기 노출 시 생태 독성 및 생리적 교란을 유발할 수 있음을 시사한다. Li은 먹이사슬을 통해 생물체 내에 단계적으로 축적되며 생태계 전반에 영향을 미칠 수 있고, 장기적으로는 신장 질환과 심혈관계 이상, 유전 독성 등 인간 건강에도 위해를 초래할 수 있다(Man et al., 2024). Li은 혈중 농도를 기준으로 약 10 mg/L 수준에 도달하면 경미한 중독 증상이 나타나며, 15 mg/L 수준에서는 언어 장애와 함께 사망 위험이 증가하는 것으로 보고되었다(Aral and Vecchio-Sadus, 2008).
이러한 잠재적 위험성에도 불구하고 현재까지 Li에 대한 환경 기준은 국제적으로 명확히 확립되지 않았으며, 환경 내 Li 거동에 대한 연구도 부족한 실정이다(Oliver and Hewett, 2024). 기존 연구는 대부분 농도 기반의 단순 모니터링에 국한되어 Li 오염의 기원을 정량적으로 규명할 수 있는 추적 기법이 부족하였다. 이러한 한계를 해결하기 위한 접근으로 최근 Li 동위원소를 활용한 기원 추적 기법이 주목받고 있다(Choi et al., 2019; Négrel et al., 2020; Millot and Négrel, 2021; Desaulty et al., 2022). Li은 자연계에서 6Li (약 7.5%)과 7Li (약 92.5%) 두 안정 동위원소로 존재하며, 약 17%의 큰 질량 차이에 의해 다양한 지화학적 과정에서 뚜렷한 동위원소 분별이 발생한다(Vigier et al., 2015). Li 동위원소비(δ7Li)는 시료 내 7Li/6Li의 비를 국제 표준물질(L-SVEC)과 비교하여 나타낸 값으로, δ7Li = [(7Li/6Li)_sample / (7Li/6Li)_L-SVEC − 1] × 1000의 수식으로 계산된다(Choi et al., 2019). δ7Li 값은 환경 내 Li의 기원과 이동 경로를 정량적으로 규명할 수 있는 유용한 지화학적 추적자(geochemical tracer)로 활용될 수 있다(Tomascak et al., 2016; Ryu and Vigier, 2024).
이 논문은 Li의 환경 내 거동, 생물학적 축적 및 생리적 영향, 동위원소 조성을 활용한 기원 추적 가능성에 관한 최신 연구 동향을 통합적으로 고찰함으로써, Li 오염에 대한 과학적 이해를 향상시키고, 향후 환경 기준 설정 및 관리 전략 수립을 위한 기초 자료를 제공하는 것을 목적으로 한다. 이를 위해, (1) 자연적 및 인위적 기원에 따른 Li의 주요 발생원과 수계 내 농도 분포 특성을 정리하고, 지질학적 배경과 산업·생활계 활동에 따른 농도 변화 양상을 비교함으로써 환경 중 Li의 분포 특성과 주요 유입 경로를 고찰하고자 한다. 다음으로, (2) 수생 생물과 육상 식물에서 보고된 생물학적 축적 양상과 생리·독성 반응을 분석하여 종별 노출 민감도와 생태학적 영향을 평가하고, (3) 지표환경에서 Li 동위원소(δ7Li)가 분별되는 주요 지화학적 메커니즘을 정리하여 자연적 기원에 따른 δ7Li 조성의 특징을 이론적으로 규명하고자 한다. 마지막으로 (4) 하천, 도시 수계, 하수 및 산업 배출원 등 다양한 인위적 오염원에서 보고된 δ7Li 조성 특성을 비교 분석함으로써, Li 동위원소 기반 기원 추적 기법의 적용 가능성과 한계를 평가하고자 한다.
리튬 주요 발생원과 수계 내 농도 분포
자연적 기원
수계 내 Li 농도는 지질학적 특성에 따라 다양하게 나타나며(Table 1), 수계 유형에 따라 수 µg/L에서 수십 mg/L의 규모 차이를 보인다(Fig. 1). 지표수의 경우 주로 암석 풍화, 광상 분포, 열수 및 지하수 유입과 같은 지화학적 요인에 의해 결정된다. 첫째, 암석 풍화는 자연적 Li 유입의 대표적 요소이다. Li은 일반적으로 규산염암, 점토광물에 고정되어 있으나 장기간의 풍화와 수문 순환 과정으로 인해 용출되어 수계로 유입될 수 있다(Dellinger et al., 2014; Rosen et al., 2020). 강우 기원의 평균 Li은 대체로 0.48 µg/L로 매우 낮은 농도 수준이지만(Poissant et al., 1994), 현무암 풍화가 활발한 Lasa River의 평균 Li 농도는 1.2 µg/L로 보고되었으며 암석 풍화가 지표수 내 Li 조성 형성에 중요한 역할을 한다는 점을 보여준다(Pogge von Strandmann et al., 2016).
둘째, Li 광상은 자연적 Li 농도를 높이는 또 다른 핵심 요소이다. Lithium-Cesium-Tantalum (LCT)형 페그마타이트 광상이 존재하는 지역 하천의 상류에서 최대 828 µg/L까지 농도가 관찰되었으며, 약 33 km 떨어진 하류에서도 52.7 µg/L로 배경 농도(< 32 µg/L)를 상회하는 수치가 보고되었다(Williams et al., 2024). 그러나 채굴 이전 아일랜드 County Carlow 지역의 지표수는 평균 20 µg/L 수준으로 나타났으며(Kavanagh et al., 2017), 이러한 차이는 지역별 지질 특성, 지하수 유동 경로, 풍화 및 침출 강도 등 다양한 지질학적 특성이 Li 용출에 반영된 결과로 해석된다.
마지막으로, 증발 환경과 열수 및 열수 기원의 염수(brine)는 높은 Li 농도를 갖는 대표적인 자연환경이다. 사막 분지에 위치한 염호와 염수에서는 강한 증발로 인해 Li 농도가 수십 mg/L 수준까지 증가할 수 있음이 보고되었으며(Yang et al., 2024), 열수 및 염수 용출이 활발한 독일 Upper Rhine Graben 지역에서는 최대 210 mg/L의 매우 높은 Li 농도가 보고되었다(Sanjuan et al., 2016; Kölbel et al., 2023). 또한, 하구 및 기수역에서는 Li 농도가 낮은 담수와 농도가 높은 해수와의 혼합이 Li 농도 분포를 조절하는 요인으로 작용한다. 장강 하구 지역에서는 염분이 증가함에 따라 Li 농도가 뚜렷하게 상승하는 경향이 관찰되었다(Zou et al., 2024). 선행연구들을 종합한 결과, 자연적 기원의 지표수 내 Li 농도는 수 µg/L에서 수십 µg/L 수준의 배경농도로 유지됨을 확인하였다. 또한 LCT형 페그마타이트, 염호, 열수, 염수 등 다양한 지질학적 조건에 따라 Li 농도가 수백 µg/L에서 수십 mg/L 수준까지 크게 증가할 수 있으며, 이는 자연적 Li 조성이 지질 환경과 기후 특성에 따라 매우 다양하게 나타날 수 있음을 보여준다.
지하수 내 Li 농도 역시 지질학적 특성에 따라 큰 변동성을 보인다. 호주 Darling River 충적대수층에서는 지하수와 점토광물의 상호작용에 의해 Li 농도가 약 120 µg/L 수준까지 나타났으며(Meredith et al., 2013), 카르스트(karst) 및 석회암 대수층에서는 일반적으로 수 µg/L 수준의 낮은 Li 농도가 관찰된다(Török et al., 2021). 미국 전역의 지하수를 대상으로 한 대규모 조사에서도 Li 농도는 주로 자연적 지질 요인에 의해 결정되며, 대부분의 지하수는 수십 µg/L 이하의 농도를 보이는 것으로 보고되었다(Lindsey et al., 2021).
Table 1.
Distribution of Li in natural waters
| Origin | Location of water sample | Water body | Li source | Li concentration (µg/L) | References |
| Geological | Laxa River, Iceland | River | Basalt weathering | 0.80–1.65 | Pogge von Strandmann et al. (2016) |
|
Kings Creek, just downstream of Kings Mountain Mine, NC, USA | River |
LCT-type pegmatite deposit | 52.7–828 | Williams et al. (2024) | |
| County Carlow, Ireland |
River, Stream, Groundwater |
Geological weathering | ~97 | Kavanagh et al. (2017) | |
|
Upper Rhine Graben (Germany, France) | Geothermal brine | Geothermal brine | 155,000–210,000 | Kölbel et al. (2023) | |
| Yangtze Estuary, China | River | Brine | ~189 | Zou et al. (2024) | |
| Han River (upstream), Korea | River | Silicate weathering | 0.11–0.79 | Choi et al. (2019) | |
|
Darling River alluvial aquifer, Australia | Groundwater |
Water-rock interaction | ~120 | Meredith et al. (2013) | |
| Karst aquifers, Romania | Groundwater |
Lithology-controlled weathering | 1–12 | Török et al. (2021) | |
|
United States (33 principal aquifers) | Groundwater | Geogenic sources |
~1,700 (median 6–8) | Lindsey et al. (2021) | |
|
Anthropo- genic | North Carolina | Groundwater |
LCT-type pegmatite deposit | ~46,700 | Williams et al. (2024) |
|
Flotation process water (M-BM), LIB recycling plant |
Industrial process water |
LIB recycling process water | 400,000–5,000,000 | Salces et al. (2024) | |
|
Jinjiang River, downstream of Li industrial area, China | River | Industrial activities | 30.4–103.9 | Yang et al. (2024) | |
| Han River (downstream), Korea | River | Anthropogenic inputs | 0.39–1.69 | Choi et al. (2019) |
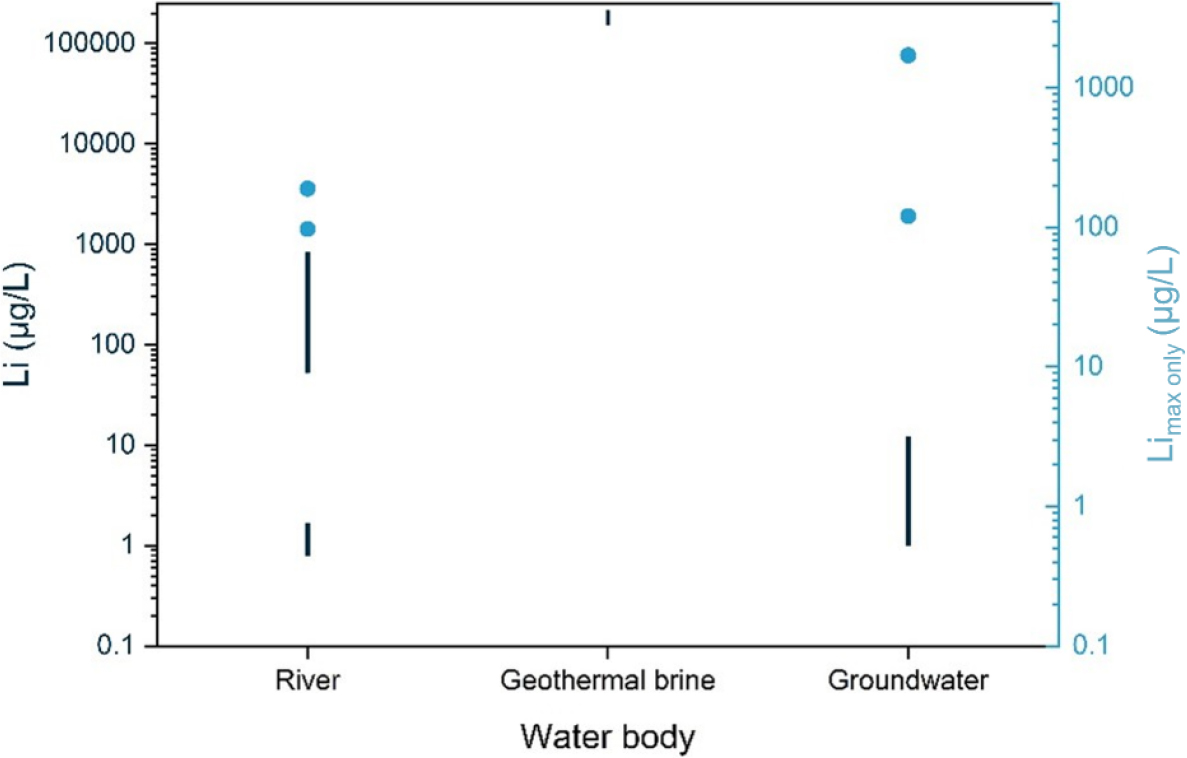
Fig. 1.
Comparison of Li concentrations across different water bodies, including rivers, geothermal brines, and groundwater, compiled from published literature. Vertical bars represent the minimum–maximum Li concentration ranges reported for individual sites or water systems, while symbols indicate cases where only maximum values were available. Blue symbols plotted against the right y-axis represent maximum Li concentrations reported without corresponding minimum values. Riverine Li concentrations primarily reflect geological controls such as basalt and silicate weathering and the presence of lithium-bearing pegmatite deposits (Pogge von Strandmann et al., 2016; Kavanagh et al., 2017; Choi et al., 2019; Williams et al., 2024; Zou et al., 2024). Geothermal brines exhibit substantially elevated Li concentrations due to hydrothermal circulation and deep fluid–rock interaction (Kölbel et al., 2023). Groundwater Li concentrations show a wide range depending on lithology and water-rock interaction processes, including alluvial and karst aquifers as well as regionally extensive groundwater systems (Meredith et al., 2013; Lindsey et al., 2021; Török et al., 2021).
인위적 기원
리튬의 인위적 기원은 주로 광산 채굴과 제련, 이차전지 재활용, 도시화와 산업화로 인한 생활하수 및 폐기물 처리 과정에서 비롯되며, 이러한 활동은 수계로의 지속적인 Li 유입을 증가시켜 수질 오염의 잠재적인 원인이 된다(Kavanagh et al., 2017; Mrozik et al., 2021). 특히 Li 채굴 및 제련 과정에서 발생하는 광산 폐기물은 대표적인 인위적 배출원 중 하나이다. 경암형(hard rock) Li 광상에서 발생되는 폐석과 광미는 일반 토양보다 높은 Li 농도를 지니며, pH 변화나 산화·환원 조건에 따라 용출되는 Li 농도가 급격히 증가될 수 있다. Williams et al. (2024)은 미국 North Carolina의 경암형 Li 광산 인근에서 지하수 내 Li 농도가 최대 46,700 µg/L, 평균 41.2 µg/L로 배경 농도인 7 µg/L를 크게 상회함을 보고하였다. 이러한 결과는 광산 폐기물로부터 용출된 Li이 인근 지하수 및 지표수로 확산될 수 있음을 보여주며, 채굴 활동이 Li의 환경 내 이동과 장기적 잔류에 중요한 영향을 미칠 수 있음을 시사한다.
이차전지 산업의 급속한 성장은 최근 Li 오염의 주요 요인으로 부각되고 있다. Li은 LIB 양극재를 제조하는 과정에서 공정수로 유출될 수 있으며, 사용 후 LIB는 구성 부품의 복합성과 높은 화학적 안정성으로 인해 완전한 분해가 어렵다. 따라서 부적절한 처리나 단순 매립이 이루어질 경우, Li이 토양과 지하수로 용출되어 환경 오염을 유발할 수 있다(Mrozik et al., 2021). 실제로 Richa et al. (2017)은 사용 후 LIB를 매립할 경우 약 42.5%의 Li이 침출수로 용출될 수 있음을 보고하였고, LIB 재활용 과정에서 발생하는 공정수와 세정수의 Li 농도는 400–5,000 mg/L 범위로 보고되었다(Salces et al., 2024). 이러한 고농도의 폐수가 적절한 처리 없이 외부환경으로 방류될 경우, 토양과 지하수 오염의 직접적인 원인이 될 수 있다. LIB 재활용은 기계적 전처리, 열처리, 습식 제련 공정이 단계적으로 수행되며, 이 과정에서 다양한 형태의 폐수가 발생한다. 특히, 열처리 과정에서 전극 내 Li 화합물이 수용성 형태로 전환되어 공정수로 용출되고, 해당 공정수가 폐수로 전환된 뒤 적절히 처리되지 않을 경우 지표수로 유입되어 Li 오염의 주요 요인으로 작용할 수 있다(Salces et al., 2024).
추가적인 Li의 유입 경로로는 도시화와 산업화에 따라 증가하는 생활기원 오염원이 있다. Li은 윤활유, 유리, 세라믹, 항우울제 등 다양한 산업, 생활, 의학용품의 원료로 사용되기 때문에 도시지역에서는 생활하수 내 Li 농도가 높게 나타난다(Choi et al., 2019). Li 배출을 저감하기 위해 하수처리시설이 운영되고 있으나, Pinter et al. (2022)에 의하면 북미 오대호 유역에서 35개 하수처리장의 Li 제거 효율 평균은 15%에 불과한 것으로 보고되었다. 일부 정수 처리시설에서는 처리수와 하천수의 Li 농도가 유사하게 나타나 정수 처리 과정에서 Li 제거 효율이 낮은 것으로 나타났다(Yang et al., 2024). 이는 기존 하수·정수처리 공정에서 Li이 대부분 제거되지 않은 채 수계로 방류되고 있음을 시사한다. 도시 생활하수 외에도 산업 활동이 집중된 지역에서는 하천 내 Li 농도가 뚜렷하게 상승하는 경향이 보고되었다. 중국 진장강의 비공업 구간에서 Li 농도는 1.1–3.0 µg/L 수준이었으나 Li 산업지대를 지난 직후 103.9 µg/L로 급증하여 전반적으로 산업 활동이 하천 Li 농도를 상승시키는 주요 요인임을 확인하였다(Yang et al., 2024). 이러한 Li 분포 패턴은 산업 활동이 하천 Li 오염에 직접적인 영향을 미칠 수 있음을 시사한다.
선행 연구들을 종합하면, Li은 자연적 기원뿐만 아니라 도시화와 산업화에 수반되는 다양한 인위적 배출원을 통해 수계 전반으로 광범위하게 확산될 수 있는 것으로 보고된다. 특히 사용 후 LIB의 매립 및 재활용 공정에서 발생하는 고농도 Li 함유 폐수와 하·폐수처리시설의 낮은 Li 제거 효율은 Li의 수환경 내 장기 잔류 및 축적 가능성을 증대시키는 주요 요인으로 지적된다. 이러한 점은 수계에서의 Li 농도에 대한 체계적 모니터링을 강화함과 동시에 Li을 대상으로 엄격한 관리 기준 및 규제 체계의 정비가 필요함을 시사한다.
수생 동물 및 육상 식물에서의 생물학적 Li 축적 및 독성 영향
수생 동물에서의 Li 축적 및 독성 반응
수생태계에서 Li은 주로 용존 이온 형태로 존재하여 수생 생물에 대한 노출 반응이 빠르게 나타나는 것으로 알려져 있다(Kszos and Stewart, 2003). 이러한 특성으로 인해 수생 생물은 Li 오염의 생물학적 축적과 독성 반응을 평가하는 대표적인 지표군으로 활용된다. 어류와 무척추동물은 수계 내 Li의 생태학적 영향을 평가하기 위한 핵심 지표생물군이다. 어류는 아가미와 피부를 통한 직접 흡수뿐만 아니라 먹이망 상위 단계에 위치함으로써 먹이 사슬을 통한 Li의 축적 가능성을 반영할 수 있어 생태계 수준의 영향을 평가하는 데 유리하다(Thibon et al., 2021). 실험 연구에서는 투명한 배아와 빠른 성장 특성을 지닌 제브라피쉬(zebrafish, Danio rerio)가 저농도 노출 조건에서도 행동 및 생리 반응을 민감하게 탐지할 수 있어 연구에 널리 활용되며, 잉어(carp, Cyprinus carpio)는 현장 적용성과 조직별 축적 특성 평가에 적합하여 위험 평가 자료 확보에 유리하다(Hill et al., 2005). 패각류와 두족류는 높은 금속 축적 능력과 환경 변화에 대한 민감한 반응성으로 인해 Li의 생물학적 축적과 독성 평가에 효과적인 지표군으로 평가된다. 패각류는 연조직 내 Li 축적이 용이하고 생물농축계수(bioconcentration factor, BCF) 산정에 적합하다(Zuykov et al., 2013; Schöne and Krause Jr, 2016). 두족류는 높은 대사율과 발달한 신경계로 인해 단기 노출에서도 조직 내 높은 금속이온류 축적과 효소 활성 변화, 이온 교란을 보이며, 먹이 기반 노출 평가를 통해 Li의 단계별 전이 가능성까지 검토할 수 있다(Penicaud et al., 2017).
Nery et al. (2014)은 Li 노출이 척추동물의 신경발달 및 행동학적 역량에 미치는 영향을 규명하기 위해 제브라피쉬 배아를 이용한 노출 실험을 수행하였다. 연구에서는 야생 제브라피쉬를 교배시켜 수정 직후의 배아를 확보한 뒤, 0, 0.05, 0.5, 5.0 mM 농도의 염화리튬(lithium chloride, LiCl) 용액에서 3일 동안 노출 실험을 수행하였다. Li 노출 단계가 종료된 후 모든 개체를 Li이 제거된 용액으로 옮겨 10일까지 회복 단계를 거쳐 사육하였다. Li 노출 단계 동안 생존율, 부화 시점, 형태학적 이상 여부를 관찰하였고, 사육 종료 후에는 운동성 지표를 정량화하기 위해 신경행동학적 변화를 분석하였다. 각 단계 종료 시점의 개체에서는 단백질 발현 분석(western blot)을 통해 β-catenin 등의 단백질 수준을 정량화하여, 세포 신호전달·발달 및 조직 안정성의 교란 여부를 검증하였다. Li 노출 결과, 유의미한 치사율 증가와 기형 현상이 나타나지 않았으나(p = 0.6988), 사육 종료 후의 개체군에서 Li 농도에 비례하여 이동거리(distance traveled)가 감소하는 경향을 보였다(Fig. 2a). 단백질 발현 분석 결과, Li 노출 단계 종료 시점에서 β-catenin 단백질 발현량이 대조군보다 증가하였으며(Fig. 2b), 이는 Li이 단백질 인산화효소 활성을 억제함으로써 β-catenin 분해를 저해하고, 세포 내 신호전달 변화가 운동 능력 저하와 연관될 수 있음을 시사하였다. 사육이 종료된 10일 시점에서 β-catenin 단백질 발현량은 대조군 수준으로 회복되었다(Fig. 2c). 해당 연구는 단기간의 Li 노출로도 세포 내부 체계가 일시적으로 교란될 수 있으며, 이후 신경계 발달과 행동에 장기적인 영향을 남길 수 있음을 입증하였다.
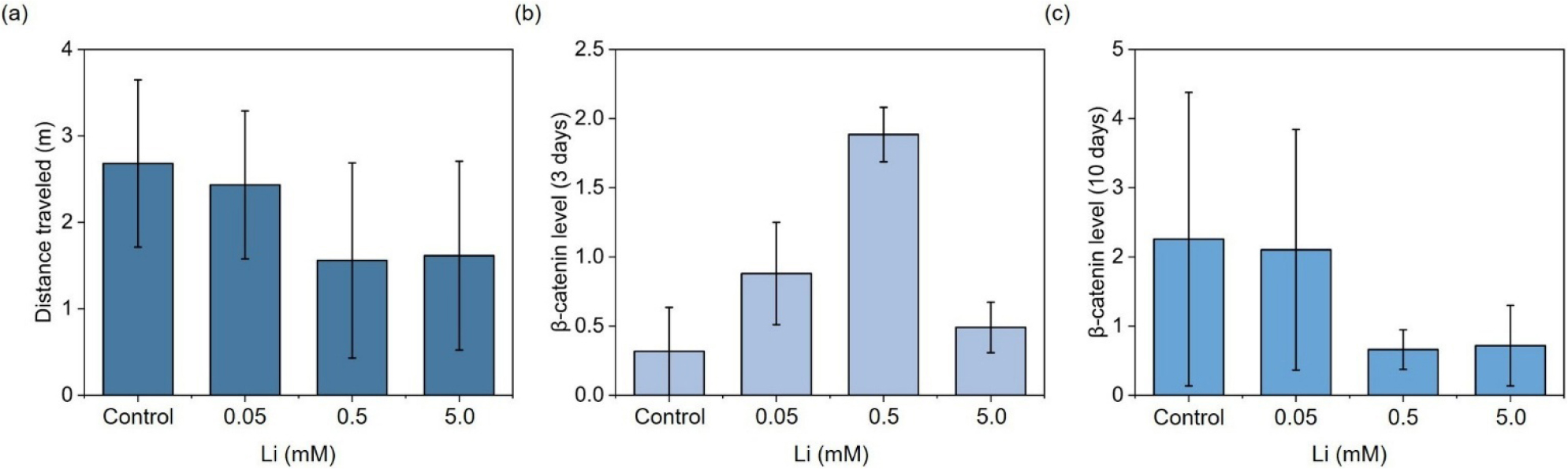
Fig. 2.
Results of Li exposure in zebrafish embryos. (a) Total distance after Li exposure in a behavioral test, (b) western blot analysis of β-catenin at 3 days, and (c) β-catenin level at 10 days. Bars represent mean values for each Li treatment, with error bars indicating standard deviation. Panels (a–c) show responses at different behavioral and molecular endpoints following exposure to increasing Li concentrations (modified from Nery et al., 2014).
Jing et al. (2021)은 Li 오염이 담수어인 잉어의 신장 조직(kidney tissue)에 미치는 독성학적 영향을 규명하기 위해 신장 내 산화적 손상(oxidative damage) 및 염증 반응을 분석하였다. 양식된 잉어 20마리를 대상으로 노출군은 20 mg/L Li 용액에서 30일간 사육하였으며, 대조군은 일반 수조에서 동일 기간 사육하였다. Li 노출 종료 후 모든 개체의 신장 조직을 채취하여 Li 농도를 측정하고, 지질 과산화 산물(malondialdehyde, MDA)을 조사하여 산화 스트레스로 인한 세포막의 손상 여부를 파악하였으며, qPCR (quantitative polymerase chain reaction) 분석을 통해 염증 관련 유전자 변화를 분석하였다. 연구 결과, 노출군의 잉어가 대조군에 비해 혈액(blood) 내 Li 농도가 증가하였으며, 신장 조직 내 Li 농도 또한 높게 나타났다(Fig. 3a). Li 노출군에서는 신장 내 활성산소 농도가 증가하였으며, MDA 수치가 대조군보다 높게 나타나 항산화 효소의 활성이 억제되고, 조직 내 산화적 손상이 발생하였음을 확인하였다(Fig. 3b). qPCR 분석 결과, 세포 성장과 분화를 조절하는 항염증 인자인 TGF-β (transforming growth factor-β)가 감소하여 신장 능력의 저하를 나타내었다(Fig. 3c). 해당 연구는 Li의 장기적 축적이 잉어의 신장 조직에 산화적 손상과 염증 반응을 촉진함으로써 조직 기능을 저하시킬 수 있음을 입증하였다.
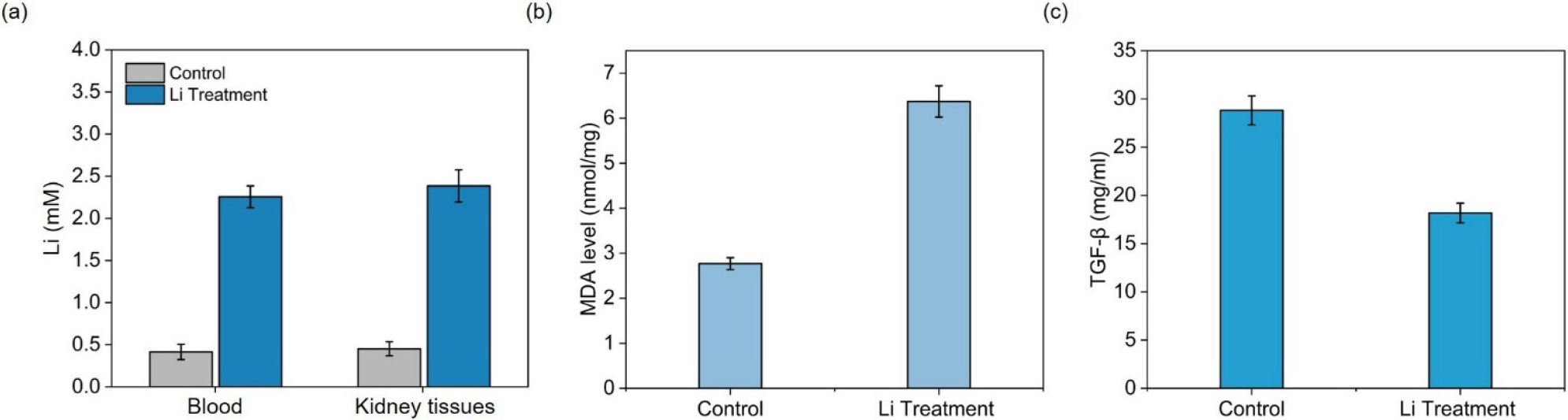
Fig. 3.
Effects of Li exposure on oxidative and inflammatory responses in carp kidneys. (a) Li content in blood and carp kidney tissue after Li exposure, (b) malondialdehyde (MDA) levels in Li-treated and control groups, and (c) expression of transforming growth factor-β (TGF-β) in Li-treated and control groups. Bars represent mean values for each group, with error bars indicating standard deviation. In panel (a), gray bars represent the control group and blue bars represent the Li-treated group; the same color scheme is applied in panels (b) and (c) (modified from Jing et al., 2021).
Campos et al. (2023)은 Li 오염이 해양 두족류의 생리·화학적 반응에 미치는 영향을 규명하기 위해 바다 달팽이(sea snail, Tritia reticulata)를 대상으로 Li 노출 실험을 수행하였다. 개체들은 0, 100, 200, 500, 1000 µg/L의 Li 농도를 갖는 해수 수조에 각각 20개체씩 배치되어 총 21일 동안 노출되었다. 노출 종료 후 각 농도에서 14개체는 생화학적 분석을 위해 액체 질소로 즉시 동결 후 Li 농도를 측정하였으며, 3개체는 행동 반응 평가를 위해 매장 행동(buring capacity) 실험에 사용되었다. 이를 기반으로 BCF를 산출하였으며, 추가적으로 에너지 대사 및 신경전달효소(acetylcholinesterase, AChE)를 측정하였다. 실험 결과, 고농도 Li에 노출된 바다 달팽이는 매장 반응 실험에서 퇴적물 속으로 더 빠르게 파고들었으며, 이는 Li과의 접촉을 최소화하려는 회피 행동으로 해석된다(Fig. 4a). 조직 내 Li 축적량은 농도 증가에 따라 증가하는 경향을 보인 반면, BCF는 농도 증가에 따라 감소하였다(Fig. 4b). 이러한 현상은 고농도 Li 환경에서 개체가 퇴적물 내부로 신속히 이동하여 수층과의 접촉 시간을 단축시키고, 결과적으로 체내 Li 흡수율을 제한하는 행동학적 조절 기전에 기인하는 것으로 판단된다. 한편 Li 노출은 에너지 대사 및 AChE 활성에 변화를 유발하지 않았으며(Fig. 4c), 이는 해당 종이 Li 독성에 대해 높은 내성을 가지고 있음을 시사한다. 해당 연구 결과를 통해 바다 달팽이가 Li에 대해 높은 내성을 보였을 뿐만 아니라, 스스로 퇴적물에 더 빨리 묻히는 회피 행동을 통해 Li의 생물축적을 효과적으로 제한하는 유용한 방어 기제를 가지고 있음이 입증되었다.
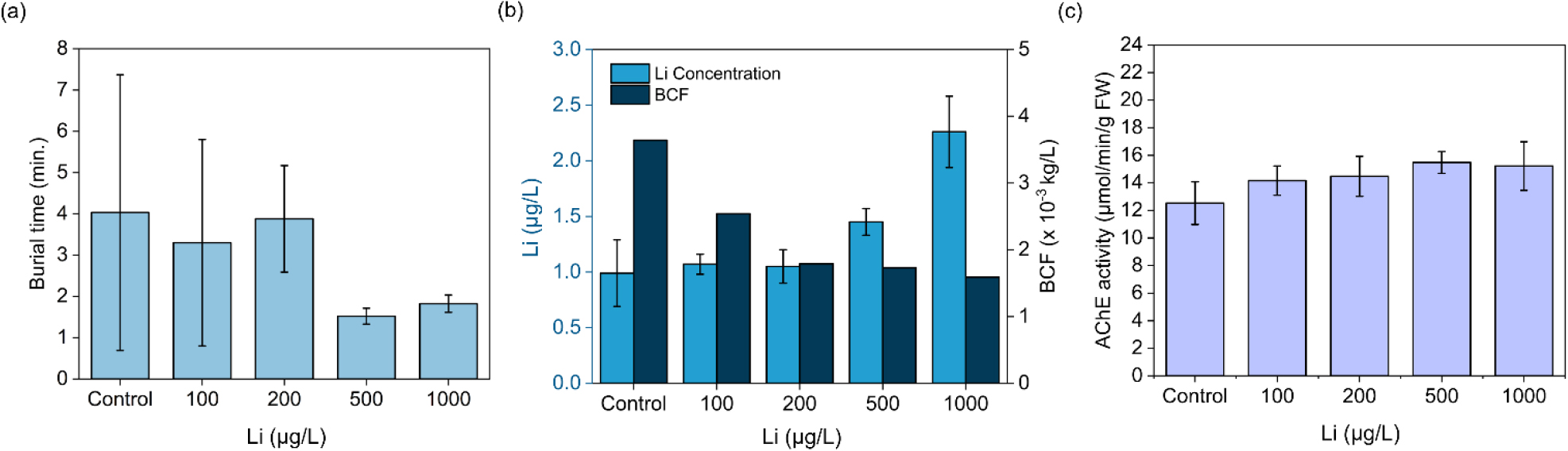
Fig. 4.
Physiological and behavioral responses of Tritia reticulata exposed to different Li concentrations. (a) Buring capacity, (b) tissue Li accumulation and bioconcentration factor (BCF), and (c) acetylcholinesterase (AChE) activity. Bars represent mean values for each Li treatment, with error bars indicating standard deviation. In panel (b), light-colored bars represent tissue Li concentrations (µg/L; left y-axis), dark-colored bars represent bioconcentration factors (BCF; right y-axis) (modified from Campos et al., 2023).
Noguera et al. (2025)은 Li의 만성 노출이 해양 패각류의 생리·조직·세포 수준에 미치는 복합적인 영향을 규명하기 위해 대표적 패각류인 지중해담치(mediterranean mussel, Mytilus galloprovincialis)를 대상으로 Li 독성 평가를 수행하였다. 스페인 Plentzia 연안에서 채집한 지중해담치를 7일간 순응시킨 후 0, 0.1, 1, 10 mg/L Li 용액에 21일간 노출시키고, 1, 7, 21일차에 아가미, 근육, 소화샘을 채취하였다. 생화학적 분석에서는 AChE와 항산화 효소인 GSTs (glutathione S-transferases), CAT (catalase) 활성을 분석하였다. 실험 결과, 지중해담치는 노출 농도와 기간의 증가에 따라 신경계, 해독계, 항산화계 효소 활성에서 농도·시간 의존적 변화를 보였다. AChE 활성은 21일차에 0.1 및 10 mg/L 처리군에서 억제되어 Li의 신경독성 반응을 시사하였다(Fig. 5a). GSTs 활성은 7일차에 10 mg/L에서 일시적으로 증가하였으나, 21일차에는 감소하여 대조군과 유사해졌고, 0.1 mg/L에서 활성이 감소하는 경향을 보여 독성 물질을 해독하는 GSTs가 Li 해독에 비효율적임을 나타냈다(Fig. 5b). CAT 활성은 1 mg/L 및 10 mg/L에서 초기 감소 후 회복되는 양상을 보였고, 저농도군에서도 7일차에 감소가 나타난 이후 21일차에 회복되는 양상을 보여 Li 노출에 대한 항산화 효소의 적응 기작을 설명하였다(Fig. 5c). 해당 연구는 지중해담치가 낮은 농도의 Li 노출 환경에서도 시간 경과에 따라 세포 및 조직 수준에서 지속적인 기능 저하가 발생할 수 있음을 시사한다.
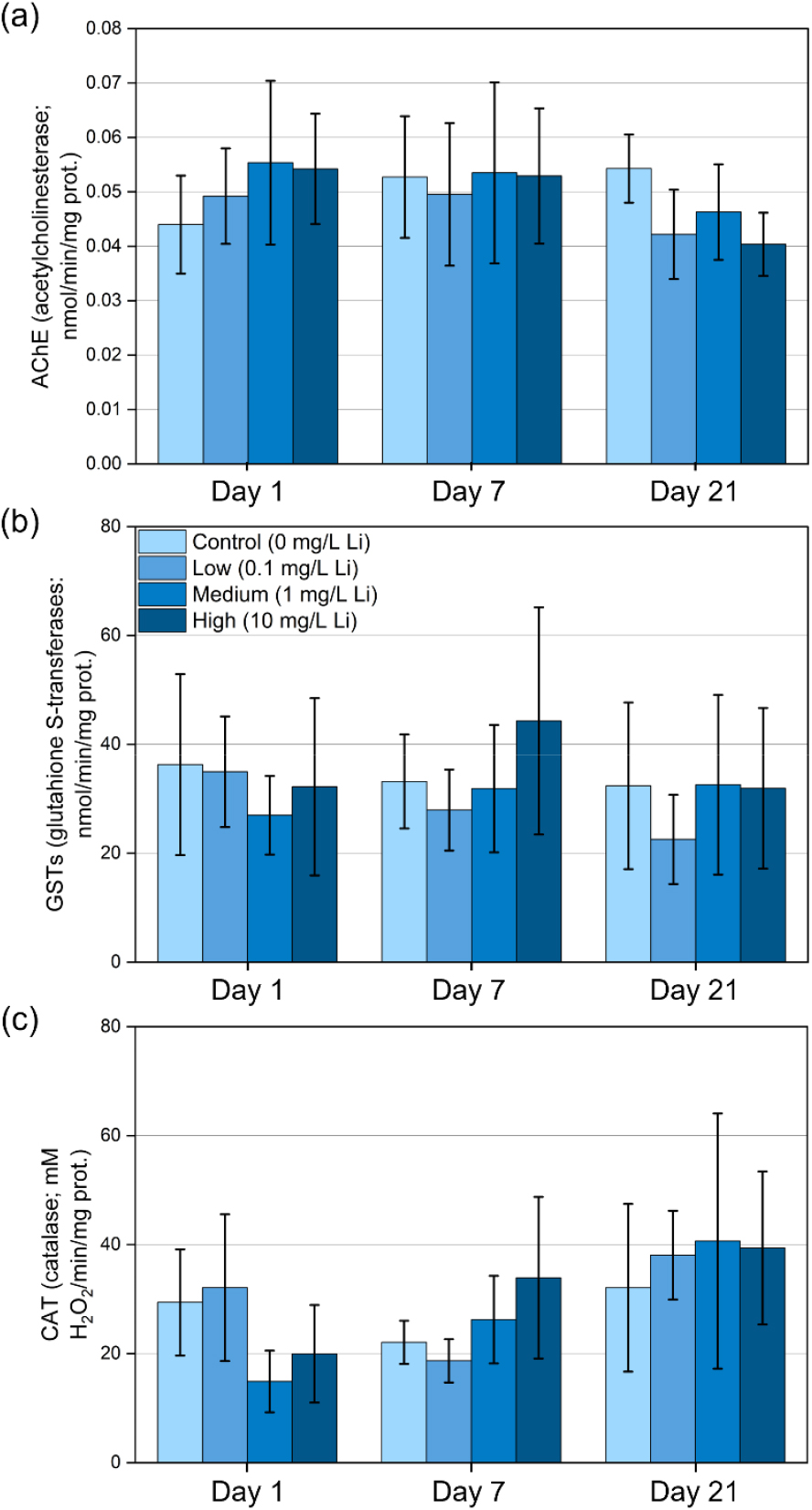
Fig. 5.
(a) AChE, (b) glutathione S-transferases (GSTs), and (c) catalase (CAT) activities in gills of Mytilus galloprovincialis after Li exposure (0, 0.1, 1, and 10 mg/L) for 1, 7, and 21 days. Bars represent mean enzyme activities for each treatment, with colors indicating Li exposure concentrations (control: 0 mg/L; low: 0.1 mg/L; medium: 1 mg/L; high: 10 mg/L), and error bars indicate standard deviation (modified from Noguera et al., 2025).
육상 식물에서의 Li 축적 및 독성 반응
식물 내 Li 축적 및 독성 반응은 식물종, Li 농도, 화합물 종류에 따라 다양하게 나타난다. 수화된 Li 이온의 반지름과 전하 특성은 K과 유사하기 때문에 식물 내에서 K 흡수 경로를 통해 뿌리 세포막을 통과하며, 체관 내 이동성이 높아 주로 지상부로 전이되는 경향을 보인다. 또한, Li 농도가 임계농도 이상으로 증가하는 경우, K과의 경쟁 흡수로 인해 식물의 생리적 대사 기능과 Li 이온의 항상성이 저하되며, 광합성 능력 저하와 함께 수분 스트레스를 유발하여 잎 괴사가 나타난다(Shahzad et al., 2016; Buendía-Valverde et al., 2024). 기관 내 Li 농도 분포는 주로 뿌리에 축적되는 경우와 지상부에 축적되는 경우로 구분되며, 이러한 차이는 뿌리에서 Li을 저장하는 정도와 체관 내 이동성 등에 의해 결정된다. Li 화합물에 결합된 음이온 종류도 흡수율과 독성 발현에 영향을 미치며, 이는 배양환경의 pH 변화, 삼투압 스트레스, 용해도 차이 등과 함께 작용하여 독성 발현을 조절한다(Kalinowska et al., 2013; Garcia-Daga et al., 2025). 따라서 Li의 식물 독성은 Li 화합물, 이온 간 경쟁, 조직별 Li 분포와 이동 특성이 복합적으로 작용한 결과로 볼 수 있다.
Franzaring et al. (2016)은 독일 남서부 지역에서 채집한 메밀(buckwheat, Fagopyrum esculentum), 옥수수(corn, Zea mays), 강낭콩(garden bean, Phaseolus vulgaris)을 대상으로, 토양의 Li 화합물 형태에 따른 조직 내 Li 축적 특성을 비교하고, Li 농도별(0, 8, 40, 80, 200, 400 mg/kg) 생물학적 반응이 대조군 대비 50% 수준으로 변화하는 반수 영향농도(median effective concentration, EC50)를 비교하였다. 연구 결과, 400 mg/kg 노출 조건에서 LiCl 노출군은 탄산리튬(lithium carbonate, Li2CO3) 노출군보다 Li 함량이 1.2배 높게 나타났으며(Fig. 6a), 이는 동일한 농도 노출 조건에서 Li 화합물 종류에 따라 토양에서 식물체 내 Li 축적 특성이 다르게 나타날 수 있음을 시사한다. LiCl 노출군에서 옥수수의 EC50는 118 mg/kg, 강낭콩과 메밀은 각각 55 mg/kg, 47 mg/kg으로 나타났다(Fig. 6b). 결과적으로, 옥수수는 동일한 노출군에서 강낭콩과 메밀에 비해 EC50이 높아, 상대적으로 Li에 대한 내성이 큰 작물로 평가된다. 이러한 결과는 옥수수가 Li으로 오염된 토양에서 다른 작물에 비해 비교적 높은 내성을 보이는 종이며, 향후 Li으로 오염된 토양에서 생리·생태 변화 연구에 유용한 지표종으로 활용될 수 있음을 시사한다.
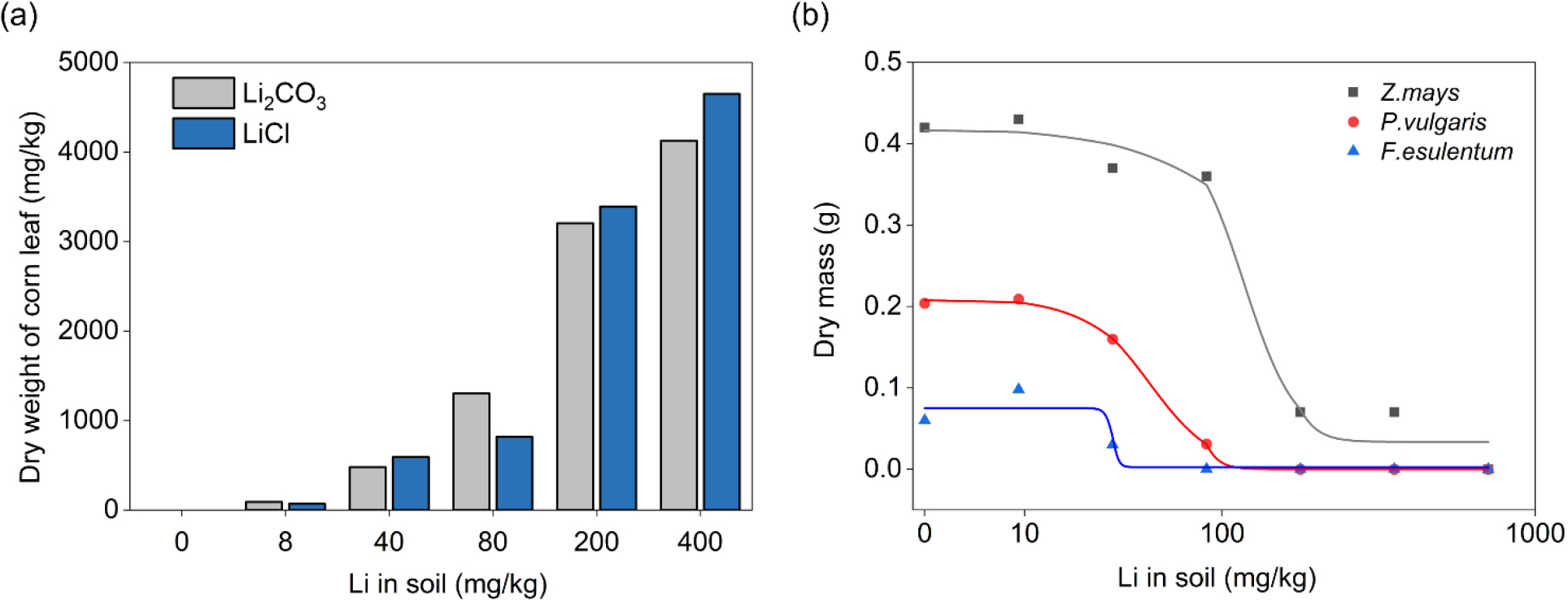
Fig. 6.
(a) Lithium concentration in corn leaves, expressed on a dry weight (DW) basis (mg/kg DW), as a function of soil Li conctent (0–200 mg/kg) under Li carbonate (Li2CO3) and Li chloride (LiCl) treatments. (b) Dose-response curves showing changes in the dry mass of shoots of Zea mays, Phaseolus vulgaris and Fagopyrum esculentum with increasing soil Li content, with corresponding median effective concentration (EC50) values of 118, 55, and 47 mg/kg, respectively. The solid lines represent the fitted content-response curves. In panel (a), gray bars represent Li2CO3 treatments and blue bars represent LiCl treatments. In panel (b), square, circle, and triangle symbols represent Zea mays, Phaseolus vulgaris, and Fagopyrum esculentum, respectively (modified from Franzaring et al., 2016).
Kalinowska et al. (2013)은 상추(lettuce, Lactuca sativa)를 대상으로 수경재배 조건에서 LiCl과 수산화리튬(lithium hydroxide, LiOH)의 Li 농도별(2.5, 20, 50, 100 mg/L) 축적 특성과 환경 매질에서 생물체로의 물질 전이 효율을 나타내는 전이계수(transfer factor, TF)를 비교하였다. 연구 결과, LiCl과 LiOH 처리군에서 상추 내 Li 농도의 변화를 관찰하였으나 큰 차이를 보이지 않았다(Fig. 7a). 이는 화합물 형태에 관계없이 Li이 상추에 동일한 수준으로 흡수될 수 있음을 시사한다. 또한, Li은 주로 뿌리에 우세하게 축적되는 양상을 보였으나 고농도 처리군인 100 mg/L에서는 지상부의 Li 함량이 더 높게 나타났다(Fig. 7b). 이러한 결과는 고농도 Li으로 오염된 환경에서 재배된 상추는 식용부에 Li이 축적될 수 있으며, 식품 섭취를 통한 Li 노출이 증가할 수 있음을 시사한다. 다만, 이러한 노출 수준이 인체 건강에 미치는 잠재적 위해성에 대해서는 독성학적 측면을 고려한 추가적인 연구가 필요하다.
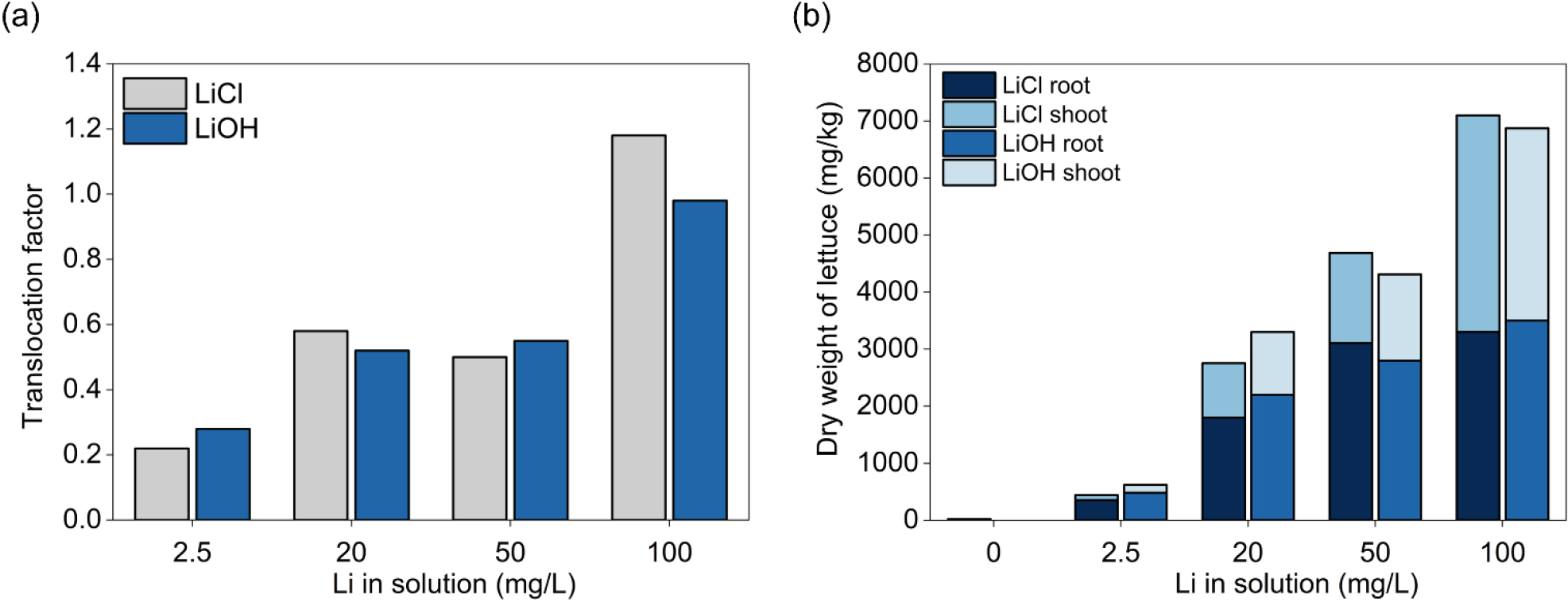
Fig. 7.
Effects of increasing Li concentrations in the nutrient solution (0–100 mg/L) on (a) Li translocation expressed as transfer factor (TF) under LiCl and LiOH treatments, and (b) Li accumulation in roots and shoots of lettuce (mg/kg DW). In panel (a), gray bars represent LiCl treatments and blue bars represent LiOH treatments. In panel (b), stacked bars represent Li accumulation in different plant compartments, with dark-colored bars indicating roots and light-colored bars indicating shoots for LiCl and LiOH treatments, respectively (modified from Kalinowska et al., 2013).
리튬의 생리·독성 반응에 대한 통합적 고찰
수생 동물 및 육상 식물에서 수행된 Li 노출 실험 결과를 종합하면, 생물종과 Li 노출 형태에 따라 Li의 생리적 반응 강도와 독성 민감도가 뚜렷하게 다르게 나타났다(Table 2). Li은 낮은 농도에서도 AChE 활성 억제, 산화적 스트레스 반응, 행동 이상 등의 생리 반응을 유발하였으며, 일정 농도 이상에서는 대사 장애, 생체 내 주요 기관의 조직학적 손상 및 운동 능력 저하가 관찰되었다. 특히 어류는 수체 내 LiCl에 노출될 경우, 신호전달 경로 교란, 신경 및 신장 조직의 구조적 손상, 유전자 발현 억제 등 빠른 생리적 반응을 보였다(Nery et al., 2014; Jing et al., 2021; Campos et al., 2023; Noguera et al., 2025). 두족류는 회피 행동을 통해 체내 Li 축적량을 제한하려는 모습을 보였고, 패각류는 AChE 및 산화 방어 체계의 교란이 보고되었다. 육상 식물의 경우 Li 농도에 따른 생체량 감소와 생장 억제가 공통적으로 관찰되었으며, Li의 화학종에 따라 흡수 및 축적 특성이 달라졌다. 이러한 결과는 Li의 독성 영향이 단순한 농도 의존성에 의해 결정되지 않으며, 노출 환경, 화학적 형태, 생물학적 기작에 의해 복합적으로 작용하여 최종 독성 반응을 조절함을 시사한다(Kalinowska et al., 2013; Franzaring et al., 2016; Shahzad et al., 2016). 따라서, Li의 생태 독성 평가에서는 단일 독성값보다는 다양한 생물학적·환경적 요인을 통합적으로 고려한 다층적 접근이 필요하다.
Table 2.
Comparative toxicity of Li in plants and aquatic organisms
| Organism type | Species | Exposure type | Threshold concentration | Effects of Li | References |
|
Aquatic (fish) | Danio rerio | LiCl | 3.45 mg/L |
Disruption of signaling pathways, behavioral disturbances | Nery et al. (2014) |
|
Aquatic (fish) | Cyprinus carpio | LiCl | 20 mg/L |
Destruction of renal architecture, suppression of mRNA expression | Jing et al. (2021) |
|
Aquatic (cephalopod) | Tritia reticulata |
Aqueous Li stock solution | 0.5 mg/L | Behavioral disturbances | Campos et al. (2023) |
|
Aquatic (shellfish) | Mytilus galloprovincialis |
Aqueous Li stock solution | 0.1 mg/L |
Reduction in AChE activity, disruption of the oxidative defense system | Noguera et al. (2025) |
|
Terrestrial (plants) | Fagopyrum esculentum, Zea mays, Phaseolus vulgaris | LiCl, Li2CO3 | 80 mg/kg | Biomass reduction | Franzaring et al. (2016) |
|
Terrestrial (plants) | Lactuca sativa | LiCl, LiOH | 50 mg/L | Shoot biomass reduction | Kalinowska et al. (2013) |
리튬 동위원소 분별 및 오염원 추적 사례
리튬 동위원소 분별의 주요 경로
리튬은 두 안정 동위원소(6Li, 7Li)로 구성되어 있으며, 지표환경에서 다양한 경로를 따라 분별(fractionation)이 발생하여 Li 동위원소 조성(δ7Li)이 변화한다. 이러한 분별 특성은 Li의 기원, 이동 경로, 반응 메커니즘을 이해하는 데 있어 유용한 추적 지표로 작용하며(Ryu and Vigier, 2024), 환경 내에서 분별이 발생하는 대표적인 경로는 다음 네 가지로 구분된다.
첫째, 주광물의 용해(primary mineral dissolution)는 Li이 암석에서 용출되는 초기 단계이다. 그러나 상대적으로 동위원소 분별은 적게 발생하며, 이는 용해가 평형 조건에서 빠르게 일어나는 반응이기 때문이다. 실제 δ7Li 조성의 주요 변화는 이차광물(secondary minerals) 형성, 점토광물에 대한 수착(sorption), 또는 탄산염 침전(carbonate precipitation) 등과 같은 후속 반응에 의해 유도된다(Ryu and Vigier, 2024). 둘째, 암석 풍화 과정에서 용출된 Li이 점토광물이나 산화물과 같은 이차광물로 재고정될 때, 이차광물의 결정격자나 표면 구조는 6Li을 선택적으로 포획하는 경향이 있다. 이러한 분별은 각 상의 결합 환경과 배위수 차이에 기인하며, 가벼운 6Li은 고배위 결합 환경을 선호하기 때문에 광물 표면이나 격자 내에 더 잘 포획된다(Schauble, 2004; Penniston-Dorland et al., 2017). 이로 인해 용액상에는 상대적으로 7Li이 농축되어 δ7Li 값이 상승하며, 이러한 평형 분별은 지표수와 지하수의 Li 동위원소 조성에서 뚜렷하게 관찰된다(Vigier et al., 2008). 셋째, 점토광물이나 산화물 표면에서 일어나는 수착 반응도 중요한 동위원소 분별 기작이다. 점토광물과 산화물의 표면은 음전하를 띠기 때문에 양이온을 끌어당기며, 이 과정에서 6Li이 7Li에 비해 더욱 효과적으로 수착된다. 이러한 선택적 수착은 단발성 반응에 국한되지 않으며, Li이 광물 표면에 교환 가능한 형태로 존재하여 반복적인 수착-탈착이 가능한 환경에서도 지속적으로 작용하는 것으로 보고되었다(Pistiner and Henderson, 2003). 이는 시간이 지남에 따라 용액 내 δ7Li 값을 점진적으로 증가시키는 주요한 분별 기작이 될 수 있다. 넷째, 탄산염 침전 과정은 pH가 높고 Ca2+ 또는 Mg2+과 같은 양이온이 풍부한 알칼리 환경에서 주로 발생하며, Li은 방해석(calcite) 등 탄산염 광물에 함께 침전될 수 있다. 이 과정에서도 6Li이 격자 내에 우선적으로 고정되며, 7Li은 상대적으로 용액에 잔류하여 δ7Li 값이 증가하는 동위원소 분별이 발생한다(Marriott et al., 2004; Gabitov et al., 2011).
이처럼 지표 환경에서의 Li 동위원소 분별 메커니즘은 다양한 연구를 통해 규명되어 왔으며, 이러한 반응 경로는 자연적 기원의 특징적인 δ7Li 조성을 형성하는 데 핵심적 역할을 한다. 자연적 분별에 의한 δ7Li 조성은 인위적 활동에서 기원한 Li의 동위원소 조성과 뚜렷이 대비되며, 이러한 차이를 기반으로 최근 연구들은 하천 및 도시 수계에서 인위적 오염 기여도를 정량적으로 평가하는 연구들이 수행되고 있다(Choi et al., 2019; Négrel et al., 2020; Millot and Négrel, 2021).
수계 내 인위적 기원 Li 추적 사례
리튬 동위원소를 활용하여 수계 내 인위적 오염을 최초로 규명한 Choi et al. (2019)은 한강 유역을 대상으로 상·하류 하천수와 수돗물, 하수 방류수의 Li 농도 및 동위원소 조성을 분석·비교하였다. 시료는 북한강(Bukhan River, BR), 남한강(Namhan River, NR), 팔당댐 상·하류의 한강 본류(Han River, HR), 그리고 서울시 주요 하수처리장(wastewater treatment plants, WWTP) 6곳 및 서울시 전역의 수돗물 공급 지역을 포함한 총 27개 지점에서 채취하였다. 연구 결과, 한강 상류인 BR과 NR에서는 낮은 Li 농도(50.4 ± 29.2 nM)와 높은 δ7Li 값(31.4 ± 3.9‰)이 유지되었으며, 이는 규산염 풍화과정에서 예상되는 Li 동위원소 분별 기작과 일치하였다. 하류로 갈수록 Li 농도는 약 6배 증가하고 δ7Li 값은 30.1‰에서 19.2‰까지 감소하는 양상을 보였다(Fig. 8). 이러한 변화는 하류 구간에서 하수처리장 방류수가 지속적으로 유입된 결과로, 도시 생활폐수의 Li 조성이 수계에 직접적으로 반영됨을 시사한다.
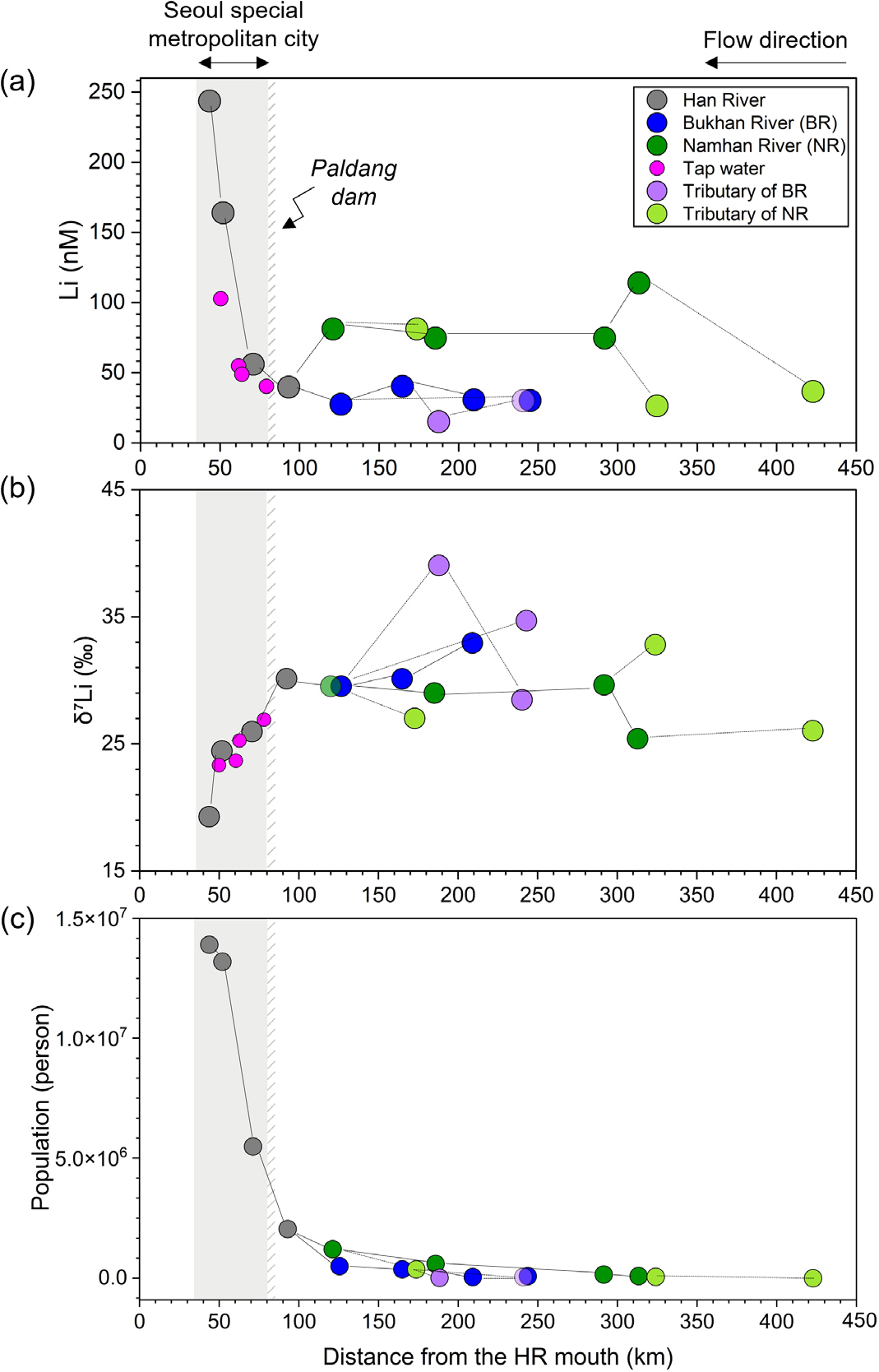
Fig. 8.
Variations in Li concentration, isotopic composition, and human population with distance from the Han River (HR) mouth. (a) Dissolved Li concentrations and (b) δ7Li values show contrasting trends across the Seoul metropolitan area, with sharp increases and decreases, respectively. (c) Population is heavily concentrated in this region, supporting the interpretation that anthropogenic activity contributes to Li enrichment and isotopic shifts in both river and tap waters. Gray circles represent Han River (HR) samples, blue circles represent Bukhan River (BR), green circles represent Namhan River (NR), purple circles represent tributaries of the BR, light-green circles represent tributaries of the NR, and pink circles represent tap water samples. Shaded areas indicate the Seoul metropolitan region, arrows denote flow direction, and lines connect sampling locations along the river system (modified from Choi et al., 2019).
하수처리장 방류수의 Li 농도는 1 mM 이상으로 매우 높고, δ7Li 값은 평균 14.5‰로 상류 하천수가 평균 31.4‰인 것에 비해 현저히 낮아 상대적으로 6Li이 풍부한 조성을 보였다. 하수처리 전·후 Li 농도 및 δ7Li 값을 비교한 결과, 농도와 동위원소 조성이 유사하게 나타나 기존 하수처리 공정이 Li 제거에 매우 비효율적임을 실증적으로 보여주었다(Fig. 9). 수돗물 역시 하천수와 유사한 Li 농도 및 δ7Li 패턴을 나타내어 정수처리 과정에서도 Li이 제거되지 않음을 확인하였다(Fig. 8). 해당 연구는 도시 생활폐수가 하천의 Li 조성에 직접적으로 반영된다는 점을 동위원소 분석을 통해 정량적으로 제시하였으며, 기존 하수·정수처리 공정에서 Li이 효과적으로 제거되지 않음을 입증하였다. 이는 앞서 언급된 Pinter et al. (2022)와 Yang et al. (2024)에서 보인 하수·정수처리 공정 중 Li 제거 효율결과와 유사함을 나타내었다.
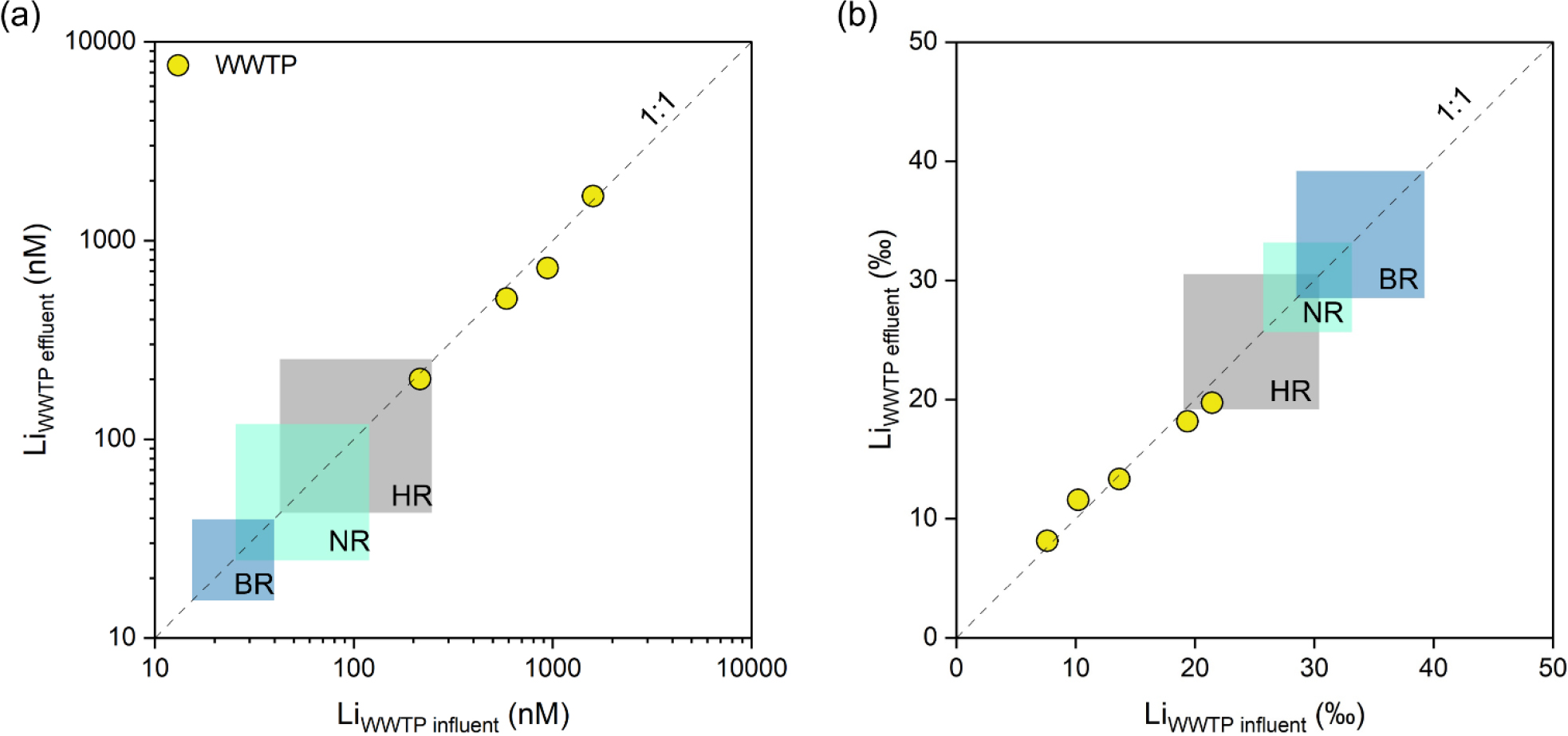
Fig. 9.
Variations in (a) Li concentration and (b) δ7Li across wastewater treatment plant influent, effluent samples. Yellow circles represent paired WWTP influent-effluent samples, and the dashed line indicates a 1:1 relationship. Shaded boxes denote the compositional ranges of river water from the Han River (HR), Bukhan River (BR), and Namhan River (NR). High Li concentrations and low δ7Li values in effluent indicate that Li is not substantially removed during wastewater treatment. Ranges for Han River and tributary samples are shown for comparison (modified from Choi et al., 2019).
하천 수계는 풍화와 인위적 오염이 복합적으로 반영된 대표적인 자연환경이다. Négrel et al. (2020)은 벨기에 북부와 네덜란드 남부에 위치한 도멜강(Dommel River) 유역을 대상으로 지표수와 지하수의 Li 농도와 δ7Li 값을 분석하여, 풍화 작용과 인위적 기원의 영향을 구분하고자 하였다. 연구 결과, 도멜강 유역의 Li 농도는 1.55–39.2 µg/L으로 전 세계 하천 평균(1.9 µg/L)보다 높았으며, δ7Li은 5.4‰에서 27.8‰까지의 넓은 범위를 보였다. 자연적 영향을 받는 지류인 Run과 Keersop에서는 Li 농도가 2.11–5.05 µg/L 수준으로 낮고, δ7Li 값은 5.4‰에서 9.4‰ 범위로 비교적 일정하게 나타나, 사질 지반에서의 규산염 풍화가 주요 Li 공급원임을 시사하였다. 하천수는 체류시간이 짧고 풍화 반응의 진행 정도가 낮아 δ7Li 값이 낮게 유지된 것으로 판단되며, Choi et al. (2019)에서 보고된 하천 수계의 평균 δ7Li 값(31.4‰)과 비교할 때 지역별 지질 특성과 체류시간 차이가 δ7Li 조성에 영향을 미친다는 점을 보여준다. 한편, 지하수의 Li 농도(1.55–4.16 µg/L)와 δ7Li 값(9.7–11.7‰)은 지류 하천수보다 높은 동위원소 조성을 보였으며, 이는 지표수에 비해 상대적으로 강한 물-암석 반응이 오랜 시간 지속된 결과로 해석된다. 상류에 위치한 제련소 배출수는 91–526 µg/L의 높은 Li 농도와 평균 26.6‰의 δ7Li 값을 보였으며, Eindergatloop 지류를 통해 본류로 유입되어 하류 방향으로 확산되며 하천수의 Li 농도 및 δ7Li 값 상승에 기여하였다(Fig. 10a). 부유물의 경우, 자연적 기원(Run, Dommel-Down)의 부유물은 Li 농도가 5–18 µg/g으로 나타났으며, δ7Li 값은 -6.4‰에서 -2.8‰로 음의 값을 보여 6Li이 고체상에 선택적으로 흡착됨을 확인하였다. 제련소 부유물은 약 11.5 µg/g의 Li 농도와 24.3‰의 δ7Li 값을 보여 7Li이 풍부한 특징을 나타냈다. 이는 용존상과 고체상 사이에 일어나는 분별을 반영하고, 인위적 기원의 Li이 하천 입자상 물질에도 영향을 미치고 있음을 시사한다. 대기 보정된 δ7Li 값과 Li/Na 비를 비교한 결과, 자연적 구간에서는 δ7Li 값과 Li/Na 비 간의 뚜렷한 양의 상관관계(R2 ≈ 0.86)가 나타나, 물-암석 상호작용과 체류시간이 풍화 강도를 결정하는 요인임이 확인되었다(Fig. 10b). 제련소 및 하수처리장의 영향을 받은 구간에서는 δ7Li이 높고 Li/Na 비가 불규칙하게 분포하여, 풍화 작용보다는 인위적 유입이 Li 조성에 지배적인 요인으로 작용함을 보여주었다. 해당 연구는 δ7Li 값과 Li/Na 비를 함께 분석하여 제련소 및 하수처리장 방류수에 의한 인위적 분별 특성을 정량적으로 구분하였다. 또한, 강수 기여 보정을 통해 Li의 자연·인위적 기원을 분리하여 해석함으로써, Li 동위원소가 다양한 환경 매체에서 오염 기원 추적 및 물질 순환 연구에 활용될 수 있음을 입증하였다.
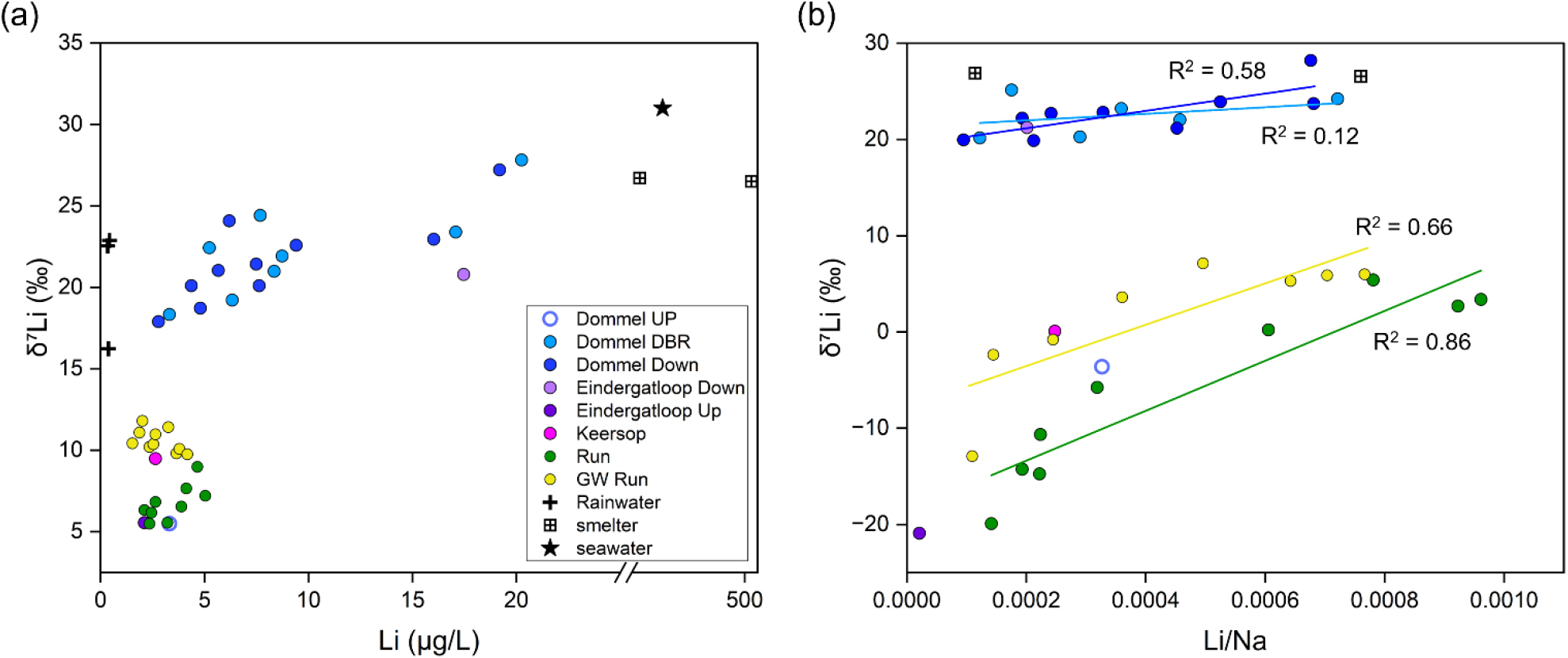
Fig. 10.
(a) Variations in dissolved Li concentration and isotopic composition (δ7Li, ‰) across surface and groundwater samples from the Dommel River basin, showing distinct enrichment in heavy isotopes in anthropogenically impacted sites. (b) Relationship between atmospheric-corrected δ7Li and molar Li/Na ratios, highlighting the contrasting controls of weathering intensity, residence time, and human input. A regression line and correlation coefficient (R2) are shown for each group. Rainwater reference data (Brest, Dax, and Orléans) are from Millot et al. (2010a, 2010b). Symbols and colors represent different water types and sampling locations, including Dommel upstream (UP), Dommel downstream of the wastewater treatment plant (DBR), Dommel downstream (Down), Eindergatloop upstream and downstream (UP and Down), Keersop, Run, groundwater from the Run catchment (GW Run), rainwater, smelter-impacted samples, and seawater (modified from Négrel et al., 2020).
Millot and Négrel (2021)은 이러한 접근법을 확장하여 자연적·인위적 오염 기여를 서로 다른 공간 규모에서 분석·비교하였다. 프랑스 루아르 강(Loire River) 유역을 대상으로 본류(약 117,800 km2)의 대규모 풍화로 인한 Li 분별을 분석하고, 오를레앙(Orléans) 인근의 소규모 Egoutier 유역(약 13 km2)에서 인위적 오염원의 영향을 평가하였다. Egoutier 유역의 시료는 상류의 자연 용출수, 병원 하류의 폐수처리장 방류수, 산업단지에서 유입되는 지류 배출수, 하천 본류에서 채취하였다. 연구 결과, 루아르 강 본류의 하천수에서 Li 농도는 2.0–46.5 µg/L, δ7Li 값은 5.0–13.3‰의 범위를 보였으며, 상류에서 하류로 갈수록 Li 농도가 증가하고 δ7Li 값이 감소하는 경향이 나타났다(Fig. 11). 이는 상류에서는 짧은 체류시간과 활발한 풍화 작용으로 인해 흡착 및 이차광물 형성에 따른 분별이 크게 나타나는 것에 비해 하류에서는 체류시간 증가와 완만한 지형으로 인해 용해가 우세하게 나타나기 때문이다. 다만, 일부 구간에서는 인위적 영향에 의해 이러한 경향에서 벗어나는 양상이 확인되었다. Andrezieux-Boutheon 지점의 경우, δ7Li 값이 주변 지점과 비교해 상대적으로 높게 나타났다. 이는 도시 및 산업폐수와 같은 인위적 요인의 영향으로 주변과 다른 경향을 보인 것으로 해석된다. 또한, 부유퇴적물의 δ7Li 값은 -8.7‰에서 -7.6‰로 하천수보다 6Li이 부화되어 나타났으며, 풍화 과정에서 이차광물 형성과 같은 반응을 통해 6Li이 고체상에 선호적으로 포획되었음을 확인하였다.
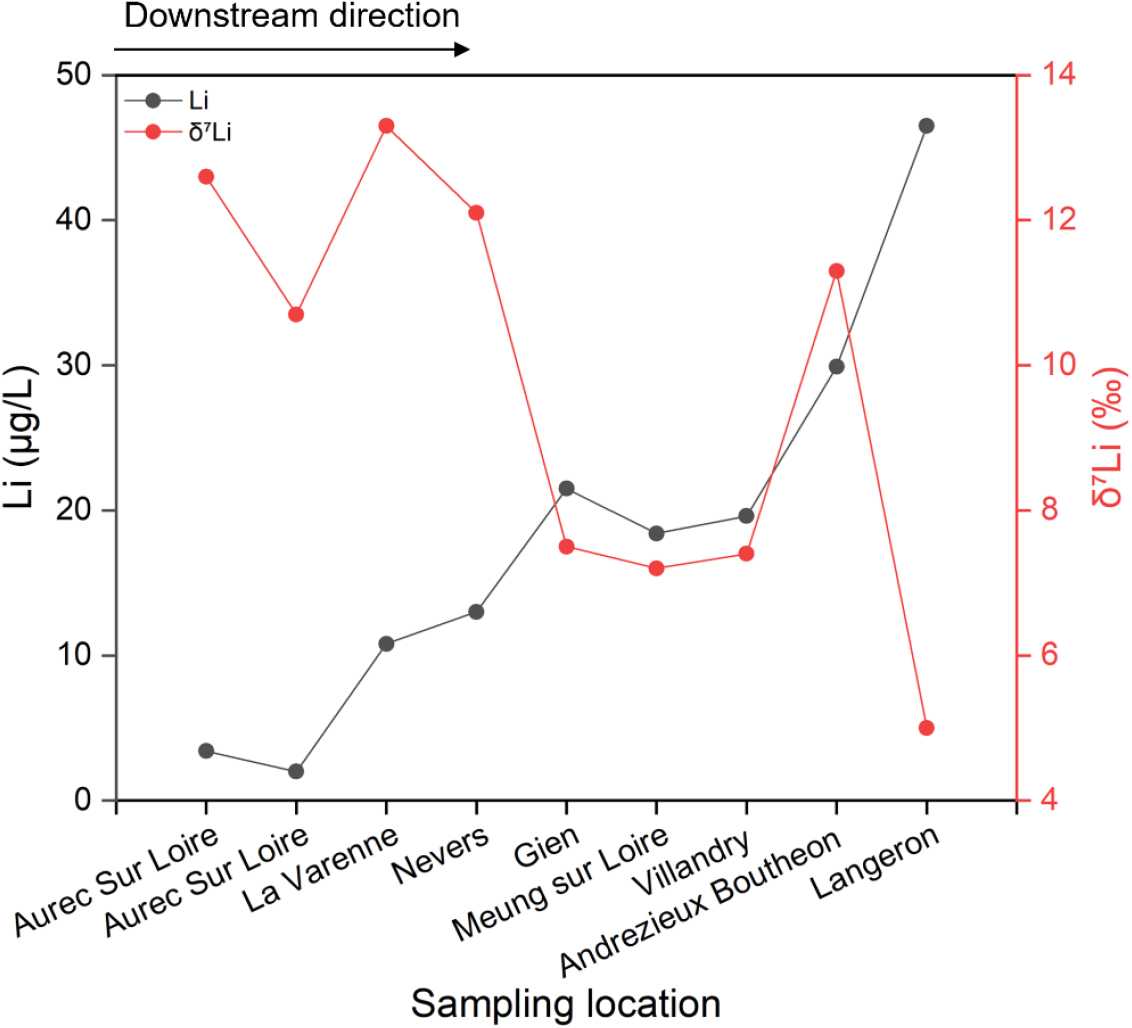
Fig. 11.
Spatial variation in dissolved Li concentration and Li isotopic composition (δ7Li) in river water along the Loire River (France), showing increasing Li concentrations and decreasing δ7Li values downstream. Black circles and the left y-axis represent dissolved Li concentrations (µg/L), red circles and the right y-axis represent δ7Li values (‰) (modified from Millot and Négrel, 2021).
Egoutier 유역 하천수의 Li 농도는 5.3–12.7 µg/L, δ7Li 값은 -3.1‰에서 4.2‰으로 나타났으며, 자연적 영향을 받는 상류 구간의 하천수는 δ7Li 값이 약 0.5‰로 일정하였고, 병원 방류수는 4.2‰, 산업단지 배출수는 -3.1‰의 상반된 값을 보였다(Fig. 12). 이러한 결과는 병원에서 치료제로 사용되는 Li2CO3이 포함된 폐수가 하천수의 δ7Li 값을 높이는 반면, 산업단지 배출수는 상대적으로 낮은 δ7Li 값을 가지는 특성이 반영된 것으로 해석된다. 또한, 하류로 갈수록 Li 농도와 δ7Li 값의 변동이 증가한 양상이 관찰되어, 인위적 오염원이 하천을 따라 확산되고 있음을 시사하였다. 해당 연구는 Li 동위원소가 광역 규모에서는 풍화·용해 과정의 지시자, 소규모 도시 유역에서는 인위적 오염의 추적자로 활용될 수 있음을 입증하였고, 하천수 내 δ7Li 값이 자연적·인위적 기원을 동시에 구분할 수 있는 다중 환경 추적 지표(dual-scale tracer)로서의 가능성을 제시하였다.
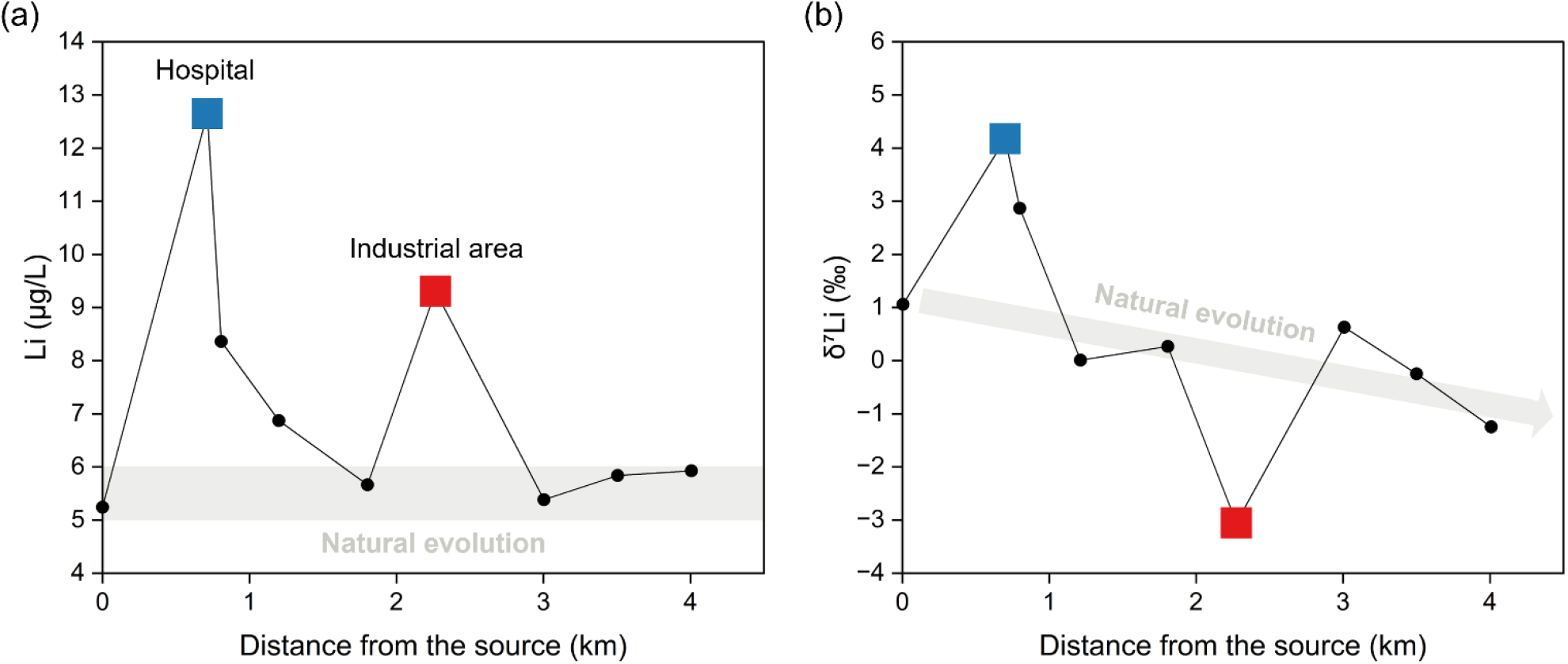
Fig. 12.
Spatial patterns of Li concentration and isotopic composition (δ7Li) in the Egoutier catchment, southern France. Black circles represent stream water samples, blue squares indicate samples influenced by hospital wastewater effluent, red squares indicate samples influenced by industrial effluents, shaded bands represent the natural background range. Distribution of (a) dissolved Li concentrations (µg/L) and (b) δ7Li values (‰) measured downstream along the stream channel from the headwater. The isotopic variability reflects inputs from anthropogenic sources, including effluent from a hospital wastewater treatment plant and nearby industrial facilities (modified from Millot and Négrel, 2021).
앞선 연구 모두 Li 동위원소 분석을 통해 수계 내 인위적 Li 오염원을 규명하였으며, 인위적 기원의 Li이 자연적 기원과 구별되는 δ7Li 값을 보이는 것이 확인되었다. 하천수에서 δ7Li 값은 오염원의 종류(산업 폐수, 하수, 제련소 배출수 등)에 따라 다르며, 공통적으로 자연적 기원과 뚜렷하게 비교되는 조성을 나타냈다. 이러한 결과는 δ7Li 값이 다양한 규모의 수계에서 인위적 오염원을 식별하고, 물질 순환을 규명하는 데 활용 가능한 신뢰성 높은 추적자임을 보여준다.
사용 후 LIB의 Li 원산지 추적 사례
리튬 이온 배터리 산업의 공급망은 원료 채굴, 정제, 양극 활물질 합성, 셀 제조로 이어지는 복잡한 다단계 공정으로 구성되어 있어, 원료 Li의 채굴 원산지를 추적하기 어렵다. Desaulty et al. (2022)은 LIB에 사용되는 Li의 지질학적 기원을 규명하기 위해 δ7Li 값을 이용한 지화학적 추적 기법을 제시하였다. 주요 Li 원산지인 남미 염수형 광상, 호주 및 중국의 경암형 spodumene 광상으로부터 생산된 Li2CO3, LiOH 등의 Li 화합물, 양극 활물질(NMC 시리즈), 그리고 완성된 셀의 양극 시트(cathode sheet)에 대한 δ7Li 값을 분석하였다. 염수형 Li은 7.9‰에서 31.4‰의 높은 값을 보인 반면, 경암형 Li은 -0.3‰에서 6.0‰의 낮은 값을 보여 명확한 동위원소 차이를 보였으며, 일부 정제 과정에서 최대 5.5‰의 분별이 확인되었다. 양극 활물질 합성 및 전지 조립 단계에서 측정된 δ7Li 값의 차이는 ± 0.4‰ 이내로 분석오차에서 동일하게 나타났다. 특히 완성된 셀의 양극 시트를 8개의 조각으로 나누어 분석한 결과에서도 10.4 ± 0.4‰로 거의 동일한 δ7Li 값이 확인되어, 제조 이후에도 원재료의 동위원소 조성이 보존됨이 실험적으로 입증되었다. 이러한 결과는 Li의 지질학적 기원이 산업 공정 이후에도 δ7Li 값에 뚜렷이 반영되어, 최종 제품 단계까지 Li 동위원소 지문으로 보존됨을 의미한다. 이를 바탕으로 연구진은 δ7Li < 6‰은 경암형으로, δ7Li > 11.3‰은 염수형으로 판정할 수 있는 1차적 기준을 제안하였다. 기준은 각 광상군의 δ7Li 분포에서 상위 75% 경계값인 Q3을 기준으로 설정되었다(Table 3). 해당 연구는 Li 동위원소 분별을 활용한 추적 기법이 블록체인이나 서류 기반 추적 시스템을 보완하는 과학적 인증 도구로 활용될 수 있으며, Li 공급망의 투명성 확보와 지속가능한 자원 관리에 기여할 수 있음을 입증하였다.
Table 3.
Ranges, medians, and upper-quartile of δ7Li values for hard-rock and brine-derived Li deposits (Desaulty et al., 2022)
인위적 Li 오염원의 δ7Li 조성 특성 비교
여러 연구에서 보고된 Li 동위원소 조성을 통해 인위적 오염원 간 조성 차이를 비교하고 오염원 추적 가능성을 평가하였다. 하수처리장 방류수(mean 14.5‰)는 상대적으로 중간 수준의 δ7Li 조성을 보였으며, 병원(4.2‰) 및 산업단지(-3.1‰) 폐수는 보다 낮은 δ7Li 값을 나타낸 반면, 제련소(mean 26.6‰) 관련 배출수에서는 높은 δ7Li 값이 관찰되었다(Fig. 13). 이는 각 오염원 원료 물질의 동위원소 조성이 반영된 결과로 해석된다. 오염원별 서로 다른 δ7Li 값 분포는 단순한 농도 차이를 넘어, 각 오염원별 고유한 동위원소 지문을 형성한다. 결과적으로 동위원소 조성 차이는 수계 내에서 서로 다른 인위적 배출원을 구별하는 데 유용한 근거를 제공한다.
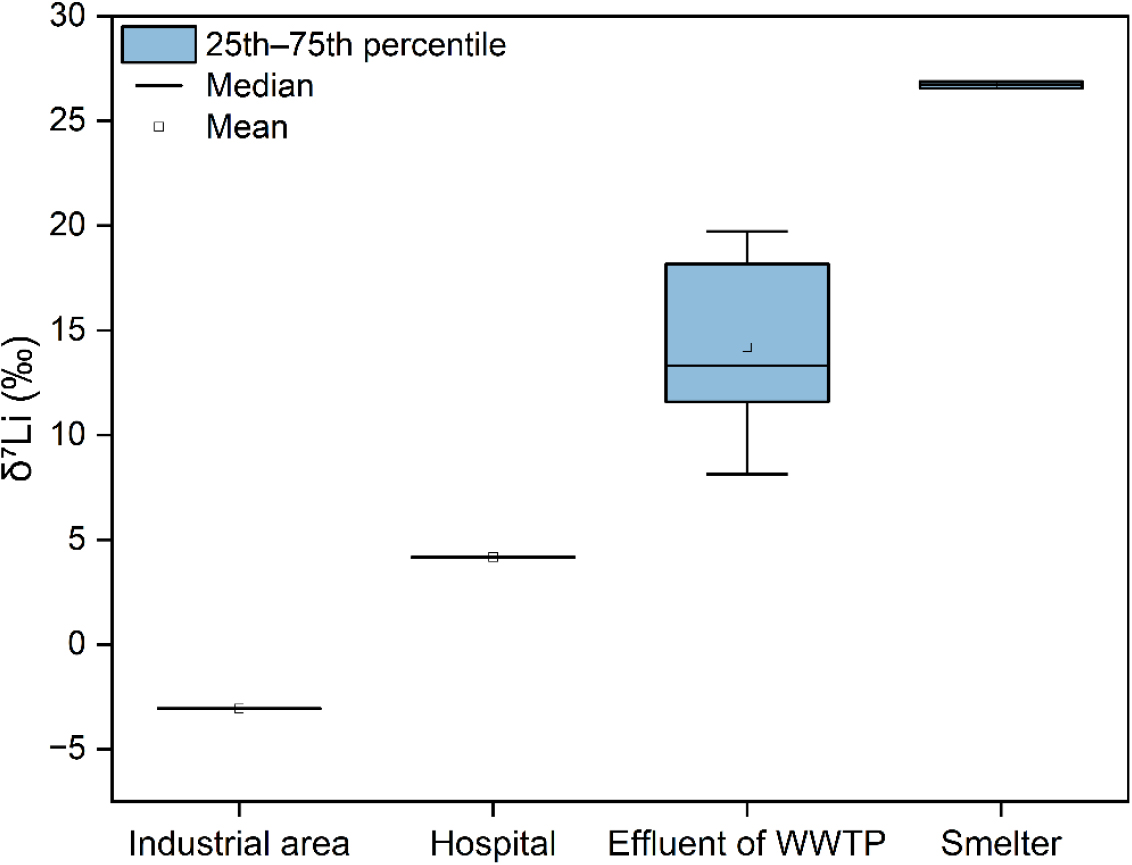
Fig. 13.
δ7Li values of Li from various anthropogenic sources, including an industrial area (-3.1‰), hospital (4.2‰), effluent from a wastewater treatment plant (WWTP; mean 14.5‰), and a smelter (mean 26.6‰) site. Data for the industrial area and hospital are from Millot and Négrel (2021), for the WWTP effluent are from Choi et al. (2019), and for the smelter runoff are from Négrel et al. (2020). Boxes represent the 25th–75th percentiles, horizontal lines indicate median values, open squares denote mean values, and whiskers show the data range.
결 론
이 논문에서는 Li 수요 증가에 따른 수계 내 Li 오염의 잠재적 위해성을 평가하기 위해 Li의 자연 및 인위적 발생원, 수계 내 농도 분포, 생물학적 축적 및 독성 반응, Li 동위원소를 활용한 오염원 추적 연구의 최신 동향을 종합적으로 검토하였다. Li의 주요 발생원은 자연적 및 인위적 기원으로 구분되며, 수계 내 Li 농도는 지질학적 특성 및 산업 활동에 따라 광범위하게 나타났다. 하수처리장 방류수, 산업 배출수 등 인위적 기원에서 유래한 Li은 자연적 기원 Li보다 수십에서 수천 배 농도가 높았으며, 현행 하수처리 및 정수처리 공정에서는 Li의 제거 효율이 낮아 수계로 직접 유입되는 것으로 확인되었다.
생태독성 측면에서, 수생 생물은 저농도 Li 노출에서도 AChE 활성 저하와 산화적 스트레스 증가가 관찰되었고, 일정 농도 이상에서는 세포 기능 교란과 운동 능력 저하가 뚜렷하게 나타났다. 시간-농도에 의존적인 패턴을 보이며, 장기 노출 시 신경계 교란 및 조직 손상으로 이어질 수 있음을 시사한다. 식물종에서는 토양 내 Li의 화학적 형태와 농도 조건에 따라 뿌리-지상부 간 축적 특성이 다르게 나타났다. 이러한 결과는 Li의 생태독성이 농도뿐 아니라 화학적 형태, 생물종에 따라 복합적으로 조절됨을 제시한다.
리튬 동위원소를 통한 오염원 추적 연구는 자연적 및 인위적 기원을 정량적으로 구분할 수 있는 유용한 도구임이 입증되었다. 지표환경에서 Li 동위원소 분별은 이차광물 생성, 점토광물의 수착, 탄산염 침전 등 다양한 지화학적 과정에서 발생되지만, 산업 배출이나 도시 하수 등 인위적 활동에서 유래한 Li은 자연적 분별 패턴과 구별된 동위원소 특성을 보였다. 이번 연구에서 기존 문헌의 δ7Li 자료를 통합 분석한 결과, 인위적 오염원별 고유한 동위원소 조성을 보였으며 이는 각 오염원별 초기 원료 Li의 동위원소 특성이 반영된 것으로 해석된다.
이번 연구를 통해 1) 도시 수계에서의 Li 오염 관리를 위해서는 배출원 규명을 넘어 수계 내 Li의 이동·변환·축적 과정을 정량적으로 파악하는 체계적 접근이 필요하고, 2) 하수처리 공정의 단계별 Li 거동 평가와 Li 제거 기술의 적용 가능성을 검토해야 하며, 3) 오염원별 동위원소 지문 데이터베이스 구축을 통해 하수처리장 방류수, 산업 배출수, 강우 유출수 등의 상대적 기여도를 정량 평가할 수 있는 참조 체계를 마련해야 하고, 4) 다양한 수생 생물군과 환경 매질에 걸친 생물축적 농도 및 독성 영향 평가를 바탕으로 과학적 근거 기반의 Li 환경 기준을 설정해야 함을 확인하였다. 향후 연구에서는 인위적 오염원 별 Li 동위원소 분별 기작에 대한 정밀 규명, 다양한 환경 조건에서의 생태독성 임계값 산정, 하수처리 공정 내 Li 제거 효율 최적화, 도시화 및 산업 활동의 영향을 받는 지역을 대상으로 장기 모니터링을 통한 Li 분포 변화 추적이 요구된다. 이와 같은 통합적 연구 체계가 구축될 경우, Li의 환경 내 순환 경로와 생태계 내 거동을 정밀하게 해석해 보건학적 영향, 장기적 수자원 관리 전략과 과학적 규제 기준 설정에 핵심적인 기여를 할 것으로 기대된다.




