서 론
세계적인 에너지 전환 정책과 전기자동차(electric vehicle, EV) 산업의 급속한 성장에 따라 리튬이온배터리(lithium-ion battery, LIB)의 수요는 전 세계적으로 빠르게 증가하고 있다(Zubi et al., 2018; Zanoletti et al., 2024). 국제에너지기구(International Energy Agency, IEA)에 따르면, 최근 약 10년간 전 세계 LIB 생산량은 256% 이상 증가하였으며, EV 보급 확대에 따라 향후에도 수요 증가는 지속될 것으로 전망된다(IEA, 2023). 이러한 LIB 사용량의 급격한 증가는 자원 소비 확대뿐 아니라 제조 공정 중 발생하는 폐잔류물과 사용 후 배터리(spent LIB)의 발생량 증가로 이어질 수 있으며(Mrozik et al., 2021), 이로 인한 Li 및 Ni, Co, Mn, Fe 등 전이금속의 환경 노출 가능성이 중요한 환경·사회적 문제로 대두되고 있다(Kang et al., 2013; Sharma and Manthiram, 2020; Mrozik et al., 2021). 특히 LIB는 금속산화물 기반 양극, 흑연 기반 음극, 유기 전해질 등 다양한 구성 요소가 결합된 복합 시스템으로 이루어져 있어(Galos et al., 2021) 자연환경에 노출될 경우 환경 변화에 따라 구성 금속의 용출 및 이동 거동이 복합적으로 나타날 수 있다(Biswal et al., 2018; Mrozik et al., 2021). 따라서 LIB 구성 물질의 환경 안정성을 평가하기 위해서는 단순한 총 함량 분석을 넘어 금속의 화학적 결합 형태 및 잠재적 이동성을 정량적으로 분석할 필요가 있다(Benson et al., 2013).
리튬이온배터리는 충·방전 과정에서 Li 이온의 삽입·탈삽입(intercalation/de-intercalation) 메커니즘을 기반으로 작동한다(Tarascon and Armand, 2001; Goodenough and Park, 2013). 일반적으로 양극재로는 층상 구조의 금속 산화물(LCO, NCM, NCA 등)이 사용되며(Chakraborty et al., 2020), 음극은 주로 흑연 기반 소재로 구성된다(Aravindan et al., 2014). LIB의 제조 공정은 슬러리 혼합, 전극 코팅 및 건조, 캘린더링, 셀 조립, 전해액 주입, 그리고 초기 활성화(formation) 단계로 이루어지며(Liu et al., 2021; Aydin et al., 2023), 이러한 공정 조건은 전극의 미세 구조와 계면 특성에 영향을 주어 장기적인 환경 노출 시 중금속 및 Li의 용출 특성에도 영향을 미칠 수 있다. 따라서 LIB 구성 성분이 환경에 노출될 경우 중금속 용출 거동을 평가하기 위해 토양 및 고형물 분석 분야에서 널리 활용되는 연속추출법(sequential extraction)이 적용될 수 있다(Tessier et al., 1979). 연속추출법은 분석 대상 금속이 시료 내에서 어떠한 결합 형태로 존재하는지를 단계별 분획(fraction)으로 구분하며, 각 분획이 특정 환경 조건에 대응할 때 나타나는 금속의 이동성을 평가하는 방법이다(Tessier et al., 1979). 이번 연구에서는 (1) 염화 암모늄(ammonium chloride, NH4Cl)을 이용한 이온교환성(exchangeable) 분획, (2) 아세트산(acetic acid, CH3COOH)을 이용한 탄산염성(carbonate) 분획, (3) 하이드록실아민 수화염화물(hydroxylamine hydrochloride, HH solution)을 이용한 산화물성(Fe–Mn oxide) 분획으로 구분하였고, 이들 분획은 각각 수계 환경, 약산성 환경(예: 산성비 또는 유기산 존재)과 산화환원 환경에서 금속 산화물이 용해되는 환경을 대표할 수 있다(Tessier et al., 1979; Biswal et al., 2024).
리튬이온배터리 내 리튬 및 중금속의 환경적 거동을 평가하기 위해서는 현재 상업적으로 널리 사용되는 대표적인 양극재 조성을 비교 분석하는 것이 필수적이며, 산업적으로 주요한 LIB 양극 시스템은 Ni·Co·Mn의 조성 비율에 따라 구분되는 NCM 계열(NCM523, NCM622, NCM811), Co 기반의 전통적 층상 구조인 LCO와 감람석(olivine) 구조 기반의 LFP 등이 있다(Zubi et al., 2018). NCM 계열은 니켈 함량 증가에 따라 에너지 밀도가 향상되는 반면(Seong et al., 2020), 구조 안정성 저하와 표면 반응성 증가로 인해 금속 용출 가능성이 상대적으로 증가하는 것으로 보고되었다(Geldasa et al., 2022; Li et al., 2024). LCO는 Co 함량이 높아 환경 위해성 평가가 특히 중요하며(Kang et al., 2013; Bozich et al., 2017; Sironval et al., 2019), LFP는 전이금속 용출 가능성이 낮고 열적·화학적 안정성이 우수하여 환경 안정성 평가를 위한 기준 물질로 활용하기에 적합하다(Barkholtz et al., 2019).
따라서 산업적 비중과 시장 대표성이 높은 세 종류의 양극재를 LIB 제조 및 폐기 과정에서 Li와 전이금속의 환경 노출 특성을 평가하기 위한 대표적인 분석 대상으로 선정한 후 연속추출실험을 진행하였다. 이를 통해 배터리 제조 잔류물 및 폐리튬이차배터리에서 Li와 전이금속이 환경 조건 변화에 따라 어떠한 분획 형태로 존재하며, 어떤 환경조건에서 우선적으로 이동·용출되는지를 규명하고자 하였다. 마지막으로 양극 조성 차이가 금속 용출 특성에 미치는 영향을 비교함으로써 향후 LIB의 환경 관리 및 순환자원화 전략 수립을 위한 과학적 근거를 제공하고자 하였다.
연구방법
양극재
이번 연구에 사용된 리튬이온배터리 양극재는 모두 상업적으로 유통되는 시판 제품으로 제조된 상용 신규 양극 소재를 사용하였다. 모든 양극재 시료는 분말 형태의 구형(spherical)이며, 리튬이온배터리 내에서 활물질(active material)로 사용되는 소재이다. NCM 계열(NCM523, NCM622, NCM811)과 LFP 양극재는 1차 입자들이 응집된 구형의 이차 입자(secondary particle) 형태이며, LCO 양극재는 주로 단 입자(single particle) 형태이다. 입자 크기는 레이저 회절법을 통해 측정된 D50 기준값을 사용하였으며, LCO는 12.1 µm, LFP는 5.0 µm, NCM523은 8.3 µm, NCM622는 11.5 µm, NCM811은 10.1 µm로 나타났다. 해당 양극재들은 배터리 내부에서 리튬 이온의 삽입·탈삽입 반응을 통해 전기 에너지를 화학 에너지 형태로 저장하는 활물질로 사용되며, 시료는 일반적으로 진공 상태 또는 비활성 기체 분위기에서 보관되는 상용 양극재의 보관 특성을 고려하여 추가적인 건조 처리는 수행하지 않았다.
NCM 양극재(NCM523, NCM622, NCM811)
NCM 계열 양극재는 니켈(Ni), 코발트(Co), 망간(Mn)을 주 구성원소로 하는 층상 구조의 Li 전이금속 산화물(LiNixCoyMnzO2)이다. 이들 소재는 Ni-Co-Mn의 조성 비율에 따라 NCM523 (x:y:z = 5:2:3), NCM622 (x:y:z = 6:2:2), NCM811 (x:y:z = 8:1:1)로 구분되며, 니켈 함량이 증가할수록 높은 에너지 밀도를 확보할 수 있는 반면 구조적 안정성이 저하되는 특징을 보인다(Voronina et al., 2020; Li et al., 2024). 일반적으로 NCM 양극재는 Ni–Co–Mn 수산화물 또는 탄산염 전구체를 공침(co-precipitation)하는 방식으로 합성한 후, 리튬 화합물과 혼합하여 고온 소성 과정을 거쳐 제조된다(Yan et al., 2015). 이러한 소재는 우수한 용량과 출력 특성으로 전기자동차용 LIB에 널리 적용되고 있으나, 높은 Ni 함량에 따른 격자 불안정성, 표면 반응성 증가 및 열화 민감성 등 구조적 한계를 동시에 내포한다(Teichert et al., 2020; Geldasa et al., 2022).
LCO 양극재
LCO (LiCoO2) 양극재는 Co 기반의 층상 구조를 갖는 Li 전이금속 산화물로 상용 LIB 중 가장 오랜 기간 사용되어 온 단일 금속계 양극재이다(Mizushima et al., 1980; Ohzuku and Ueda, 1994). LCO는 비교적 안정적인 결정 구조와 우수한 전기화학적 특성을 보이지만, 전이금속 성분이 Co 단일 원소로 구성되어 있어 환경 노출 시 코발트의 용출 특성에 대한 평가가 중요하다. 특히 산성 또는 산화·환원 조건 변화에 따라 Co 기반 산화물의 용해가 촉진될 수 있어 이번 연구에서는 연속추출법의 탄산염성 및 산화물성 분획에서 금속 거동을 비교·분석하기 위한 대표적인 대조군으로 활용하였다.
LFP 양극재
LFP (LiFePO4) 양극재는 감람석 구조를 갖는 리튬 인산철 기반 소재로 인산염(PO43-) 음이온 구조에 의해 금속–산소 결합이 강하게 고정된 형태를 가진다(Wang et al., 2011; Hovington et al., 2015). 이러한 결정 구조는 Fe의 용출 가능성을 현저히 낮추며 약산성 및 환원성 환경에서도 비교적 높은 구조적 안정성을 유지하는 것으로 알려져 있다. 이번 연구에서 LFP는 전이금속 용출이 제한적인 안정적 양극재로서 NCM 및 LCO와 비교하여 Li와 전이금속의 결합 강도 및 분획 분포 특성을 평가하기 위한 기준 물질로 활용되었다. 또한 LFP는 연속추출의 각 단계에서 금속 용출량이 가장 낮을 것으로 예상되는 대조군으로 양극재 종류에 따른 리튬 이동성 및 환경 안정성 차이를 정량적으로 비교하는 데 중요한 기준을 제공한다.
연속추출법
LIB 양극재에서 분획별 원소 조성을 구분하기 위하여 3단계 용출 및 분해 실험을 수행하였다(Tessier et al., 1979; Jang et al., 2017). 1단계에서는 1 M 염화암모늄(NH4Cl, pH = 7)을 이용하여 이온교환성 분획(exchangeable fraction)을 용출한 후, 2단계에서는 1 M 아세트산(acetic acid, pH = 5)을 이용하여 탄산염 분획(carbonate fraction)을 용출한 후, 마지막 3단계에서는 0.02 M 하이드록실아민 수화염화물(hydroxylamine hydrochloride, HH, pH = 4)을 사용하여 철-망간 산화물 분획(Fe–Mn oxide fraction)을 용출하였다. 1-2단계에서 용출된 원소는 가용성(labile) 분획으로 정의하였으며, 3단계에서 용출된 원소는 Fe–Mn 산화물 결합 분획으로 정의하였다. Fe–Mn 산화물 분획은 주로 (나노)결정질 철 및 망간 산화물 상에 결합된 원소를 반영한다.
전처리 및 분석
벌크(bulk) 양극재는 청정실험실(clean booth class 1000)에서 이차 정제된 산류(질산, 불산, 염산)을 사용하여 완전 용액화 전처리를 진행하였다. 시료 약 5 mg을 테플론 용기에 담아 불산(HF)과 질산(HNO3)을 5:3의 부피비로 혼합한 5 mL의 혼합산을 넣고 약 180°C에서 24시간 동안 시료를 반응시킨 후 용액을 증발·건고하였다. 이후 6 M 염산(HCl) 5 mL를 첨가 후 다시 180°C에서 24시간 동안 가열하여 침전된 플루오르화물(fluoride)을 제거하였다. 이후 시료를 증발 건고시킨 다음 2% 질산 10 mL로 매질을 변경하여 국립부경대학교 지구환경융합분석센터에 설치된 유도결합 플라즈마 분광분석기(inductively coupled plasma optical emission spectroscopy, ICP-OES; Optima 7000DV, PerkinElmer)를 사용하여 원소분석을 수행하였다.
각 원소의 농도 범위와 검출한계(limit of detection)를 고려한 다 원소 표준용액(Accustandard ICP-MS-CAL1-1, 2-1, 3-R-1, 4-1)을 희석하여 검량표준용액을 제작하였으며, 모든 표준용액과 시료 용액은 동일한 산 조성(2% 질산)으로 매질을 일치시켜 분석하였다. 검량곡선의 결정계수(coefficient of determination, R2)를 측정하는 모든 원소에 대해 0.999 이상으로 설정하여 검량 구간 상하에서 감도 변화에 따른 측정오차를 줄였다. 내부표준원소(internal standard element)로 Rh–In–Tl 혼합 용액을 시료와 함께 주입하여 분석 시 발생 가능한 분무기의 분무 효율 변화, 펌프 유량, 플라즈마 상태 변화 등의 장비 변화(drift)를 보정하기 위한 기준으로 사용하였다. 각 분석 배치마다 절차상 공 시료(procedural blank)을 포함하고, 공 시료의 측정 값은 각 원소별 배경농도와 검출한계 및 정량한계를 설정하는데 사용하였다. 시료 전처리 및 측정 재현성을 검증하기 위해 동일 시료를 독립적으로 전처리한 중복 시료(duplicate)를 반복 분석하여 산·시약, 전처리 용기 및 환경에서 유입될 수 있는 외부 오염원의 영향을 모니터링 하였다. 최종 농도는 전처리 및 희석 과정에서 적용된 전체 희석 배수를 곱하여 계산하였으며, 분석참고물질에 대한 정확도가 허용범위 내(±10%)에 존재하는 경우만 해당 배치의 유효한 결과로 사용하였다.
결 과
벌크 양극재
벌크 양극재의 Li 함량은 4.61–7.38 wt.% 범위로 나타났으며, Li함량은 NCM523 (7.38 wt.%) > NCM622 (7.30 wt.%) > LCO (7.25 wt.%) > NCM811 (6.87 wt.%) > LFP (4.61 wt.%)순으로 감소하였다(Table 1). 층상 구조 기반의 NCM 계열 및 LCO는 유사한 Li 함량을 가진 반면, 감람석 구조의 LFP는 상대적으로 낮은 Li 함량을 가졌다.
분획별 Li 및 전이금속 함량
분획별 Li, Ni, Co, Mn 및 Fe의 함량은 Table 1에 요약하여 제시하였다. 이온교환성, 탄산염성 및 산화물성 분획에서의 원소별 용출 범위와 양극재 종류에 따른 함량 차이는 아래와 같이 나타났다.
분획별 Li 함량은 이온교환성에서 8.92 × 101–6.59 × 103 mg/kg의 범위를 가지며, 함량은 NCM811 (6.59 × 103 mg/kg) > NCM622 (4.44 × 103 mg/kg) > NCM523 (3.09 × 103 mg/kg) > LFP (1.86 × 103 mg/kg) > LCO (8.92 × 101 mg/kg)순으로 감소하였다. 탄산염성 분획에서는 5.45 × 101–4.94 × 103 mg/kg의 범위를 가지며, 함량은 NCM811 (4.94 × 103 mg/kg) > NCM523 (2.44 × 103 mg/kg) > LFP (2.25 × 103 mg/kg) > NCM622 (1.71 × 103 mg/kg) > LCO (5.45 × 101 mg/kg)순으로 감소하였다. 산화물성 분획에서는 7.78 × 101–1.61 × 104 mg/kg의 범위를 가지며, 함량은 NCM811 (1.61 × 104 mg/kg) > LCO (2.11 × 103 mg/kg) > NCM523 (9.46 × 102 mg/kg) > NCM622 (8.37 × 102 mg/kg) > LFP (7.78 × 101 mg/kg)순으로 감소하였다.
분획별 Ni 함량은 NCM계열 양극재에서만 용출되었고 이온교환성에서 2.28 × 102–2.03 × 103 mg/kg의 범위를 가지며, 함량은 NCM811 (2.03 × 103 mg/kg) > NCM622 (3.59 × 102 mg/kg) > NCM523 (2.28 × 102 mg/kg)순으로 감소하였다. 탄산염성 분획에서 함량은 NCM811 (1.76 × 104 mg/kg) > NCM523 (4.59 × 103 mg/kg)순으로 감소하였다. 산화물성 분획에서 함량은 1.43 × 101–8.70 × 103 mg/kg의 범위를 가지며, NCM811 (8.70 × 103 mg/kg) > NCM523 (1.12 × 103 mg/kg) > NCM622 (8.55 × 102 mg/kg)순으로 감소하였고 LFP 양극재에서 1.43 × 101 mg/kg을 보였다.
분획별 Co 함량은 탄산염성과 산화물성 분획에서만 용출되었고, 탄산염성 분획에서 NCM811 (2.59 × 103 mg/kg)과 NCM523 (2.30 × 103 mg/kg) 두 양극재에서만 확인되었다. 산화물성 분획에서 함량은 1.41 × 102–1.69 × 104 mg/kg의 범위를 가지며, LCO (1.69 × 104 mg/kg) > NCM811 (1.11 × 104 mg/kg) > NCM523 (1.25 × 103 mg/kg) > NCM622 (9.89 × 102 mg/kg) > LFP (1.41 × 102 mg/kg)순으로 감소하였다.
분획별 Mn 함량은 NCM계열 양극재의 탄산염성 및 산화물성 분획에서만 확인되었다. 탄산염성 분획에서 7.06 × 102–2.49 × 103 mg/kg의 범위를 가지며, 함량은 NCM523 (2.49 × 103 mg/kg) > NCM622 (1.29 × 103 mg/kg) > NCM811 (7.06 × 102 mg/kg)순으로 감소하였다. 산화물성 분획에서 7.03 × 102–1.25 × 103 mg/kg의 범위를 가지며, 함량은 NCM523 (1.25 × 103 mg/kg) > NCM811 (7.85 × 102 mg/kg) > NCM622 (7.03 × 102 mg/kg)순으로 나타났다.
분획별 Fe 함량은 LFP 양극재에서만 용출되었다. 함량은 이온교환성에서 4.60 × 102 mg/kg, 탄산염성에서 7.79 × 102 mg/kg과 산화물성 분획에서 1.28 × 102 mg/kg이었다.
Table 1.
Elemental concentrations in different fractions bulk of LIB cathode materials
토 의
분획별 Li 분포 특성
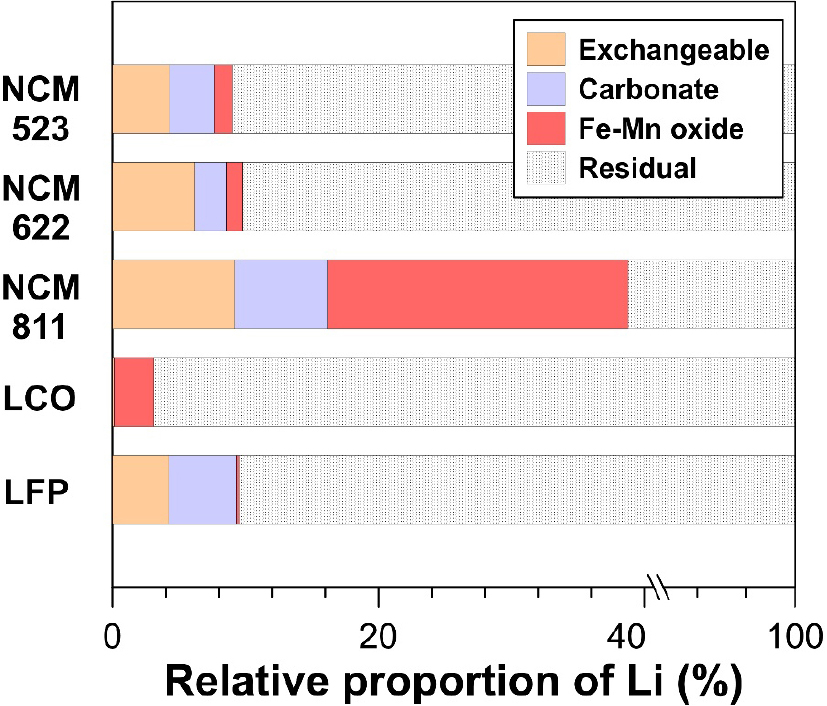
이온교환성 분획은 양극재가 환경에 노출 시 가장 먼저 용출될 수 있는 특성을 지시하며, pH 변화나 산화·환원 반응 없이도 물과의 반응만으로도 용출될 수 있어 폐양극재가 환경에 유출된 후 원소의 초기 이동성과 확산 범위를 결정하는 핵심 지표로 평가될 수 있다(Hart and Davies, 1977; Relić et al., 2010). NCM계열 중 NCM811은 이온교환성 Li 비율이 9.2%로 가장 높게 나타났으며, 이는 Ni 함량 증가에 따른 Li/Ni 치환 및 Li-O 결합 약화로 인한 격자 불안정성에 기인한다(Delmas et al., 1997). 이러한 결과는 Li이 표면 및 준표면 영역에서 완전히 고정되지 않은 상태로 존재하는 구조적 특성에 의한 것으로 판단된다. 반면 NCM523 및 NCM622는 상대적으로 낮은 Ni 함량으로 인해 구조 안정성이 유지되며, 이에 따라 이온교환성 Li 비율도 제한적으로 나타났다(각각 4.3%와 6.2%; Fig. 1). 이러한 결과는 Ni 함량 증가에 따라 LiO6 격자의 국소 왜곡에 의한 Li–O 결합 길이 증가에 의한 것으로 판단된다(Kondrakov et al., 2017). 즉, NCM계열에서 Li 이동성이 총 함량보다는 Ni의 팔면체 배위구조 변화와 이에 따른 격자 안정성에 의해 지배됨을 시사한다. 인산염 기반 PO43-–Fe 결합 구조를 갖는 LFP 양극재는 이온교환성 Li 비율이 4.2%로, 이는 Li의 대부분이 안정화된 결정격자 내 Li 자리에서 높은 결합 안정성을 유지하기 때문인 것으로 해석된다. 다만, 표면 결합 영역이나 입계에서 제한적 교환이 가능한 Li가 존재함을 의미한다. 즉, LFP 내 Li는 안정한 상태로 존재하지만 환경 내 장기 노출 및 표면 부식이 수반될 경우 상당한 용출이 일어날 수 있을 것으로 판단된다(Wang et al., 2011; Hawley et al., 2020). 이에 반해, LCO 양극재의 이온교환성 Li 비율은 0.13%에 불과하며 5개 양극재 중 이동 가능성이 가장 제한적인 소재로 확인되었다. 이는 CoO2 층상구조의 높은 결합 안정성에 의해 Li가 격자 내부에 강하게 고정되어 있어 Li 용출이 낮은 것으로 판단된다(Mizushima et al., 1980; Ohzuku and Ueda, 1994; Shkrob et al., 2017). 즉, LCO는 Li가 결정격자 내에 안정하게 고정된 구조이며, 초기 환경 노출로 인한 Li 확산 및 용출 영향은 거의 없다고 판단된다(Mizushima et al., 1980; Ohzuku and Ueda, 1994; Shkrob et al., 2017).
탄산염성 분획은 약산성 환경에서 추가적으로 용출될 수 있는 특성을 지시하며, 산성비나 이로 인해 산성화된 환경에서 쉽게 용출될 수 있는 지표로 평가될 수 있다. 탄산염성 Li 비율은 양극재별 뚜렷한 차이를 보였으며(Fig. 1), 이는 화학 구조적 특성과 결합 에너지의 차이에 의한 결과로 판단된다. NCM계열에서 용출된 Li 비율은 양극재 총 Ni 함량과 양의 상관성을 보였고(Fig. 2a), 이는 양극재 내 Ni 함량 증가에 따른 구조적 Li-O 결합력 약화에 의한 것으로 해석할 수 있다(Kasnatscheew et al., 2019). LFP에서 탄산염성 Li 비율은 5.1%로 상대적 높았으며, 이는 표면흡착 또는 약한 결합 형태의 Li+와 H+와의 치환작용에 의한 것으로 해석할 수 있다. 따라서 구조적으로 안정한 LFP가 산성 환경에 장기 노출시 잠재적 Li 오염원으로 작용할 것으로 예상된다(Goodenough and Park, 2013; Biswal et al., 2024). 이에 반해 LCO의 탄산염성 분획에서 Li는 용출되지 않았고, 이는 CoO2 층상 구조 내 Li가 강하게 결합된 상태임을 지시한다(Noh et al., 2006; Ramanujapuram et al., 2016; Qin et al., 2022). 이러한 LCO의 특성은 pH 감소만으로는 Li 용출이 일어나지 않는 강한 구조적 안정성을 의미하며, NCM 계열과 명확히 대비되는 특성이다. 따라서 LCO는 산성환경에 노출되어도 환경 내 Li 용출 가능성이 매우 제한적인 소재로 판단할 수 있다(Zubi et al., 2018).
산화물성 분획은 지하수 대수층, 토양 및 매립지 환경과 같이 산화–환원환경이 변하는 조건에서 원소들이 장기적으로 재거동될 수 있는 형태를 지시한다(Filella et al., 2003). 이 분획에서의 Li는 단기간 내 용출되기보다는 Fe 및 Mn 산화물이 환원(Fe3+ → Fe2+, Mn4+ → Mn2+)되는 과정 중 용출될 잠재성을 가진다. 즉, 이 분획은 단기 노출보다는 중·장기적인 환경 변화에 따라 용출될 수 있는 정도를 의미하며, 실제로 산화와 환원이 반복되는 지하수 대수층, 토양 및 매립지에서 발생될 가능성이 높다. 따라서 산화물성 분획은 장기적 지화학적 변화에 따른 원소 재거동 가능성을 평가하는 중요한 예측 인자로 활용될 수 있다. 이온교환성, 탄산염성 분획과 동일하게 NCM계열의 시료에서는 Ni와 Li 함량 간 양의 경향성이 관찰되지만(Fig. 2b), 이보다는 Mn과 Li 함량과의 음의 경향성으로 설명될 수 있다(Fig. 2c). 즉, Mn 환원 과정 중 표면에 흡착·공침되어 있던 Li가 함께 용출된 것으로 해석할 수 있다. LCO는 이온교환성과 탄산염성 분획에서 Li 용출이 되지 않았으나 산화물성 분획에서 Li 비율이 3.0%였다. 이는 NCM계열에서 Mn 환원에 의한 Li 용출과 유사하게 Co 환원과정(Co3+ → Co2+) 중 흡착 또는 공침된 Li가 용출된 것으로 해석할 수 있다. LFP는 산화물성 분획에서 Li 비율이 0.2%로 가장 낮은 비율을 보였다. 이는 인산염 기반 구조가 Fe-Mn 산화물 처리과정에 의해 쉽게 영향을 받지 않음을 의미하며, Li가 장기적으로 구조 내 안정적으로 결합되어 있음을 지시한다.
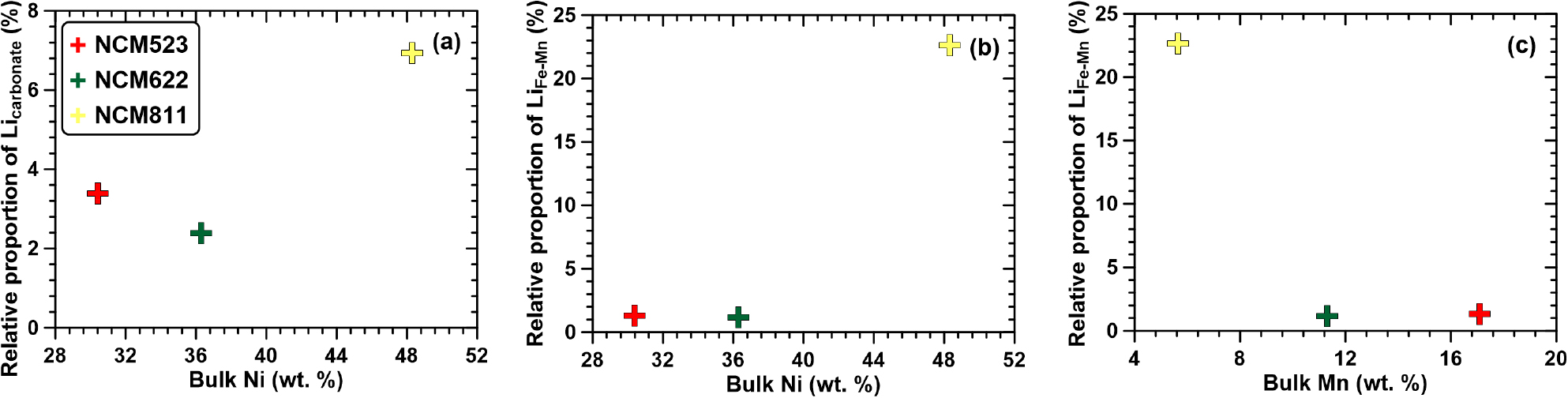
Fig. 2.
Relationships between the relative proportions of fractionated Li and bulk metal concentrations: (a) Li in the carbonate fraction versus bulk Ni concentration, (b) Li in the Fe–Mn oxide fraction versus bulk Ni concentration, and (c) Li in the Fe–Mn oxide fraction versus bulk Mn concentration.
분획별 전이금속 분포 특성
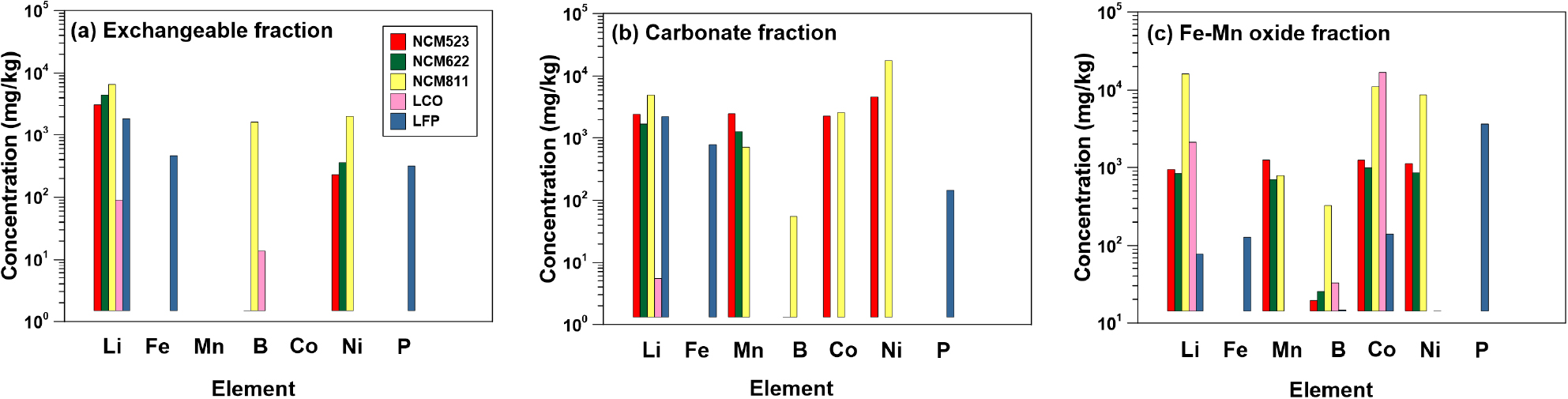
이온교환성 분획에서 전이금속은 금속–산소 결합이 상대적으로 약하거나 표면 및 준표면 영역에서 우선적으로 검출되는 것으로 보고되었다(Tessier et al., 1979; Rauret et al., 1999; Zimmerman and Weindorf, 2010). NCM계열 중 NCM811에서 Ni가 가장 높게 검출되었고, 이는 높은 Ni 함량 증가에 따라 Ni가 표면 및 준표면 영역에 상대적으로 풍부하게 분포하고, 표면 산화막 불안정성을 유발하여 이온교환 조건에서 낮은 결합 에너지 상태로 존재함을 의미한다(Julien and Mauger, 2020). 반면 Co와 Mn은 이온교환성 분획에 용출되지 않아, NCM 구조 내에서 Co–O 및 Mn–O 결합은 상대적으로 안정적 결합 상태임을 보여준다(Fig. 3a). LCO는 이온교환성 분획에서 모든 전이금속이 용출되지 않아(Fig. 3a), 강한 결합력의 CoO2 기반 층상구조를 갖는 LCO는 환경 내 이온교환성 전이금속 이동성이 가장 낮은 소재로 평가된다. LFP는 이온교환성 분획에서 Fe와 P가 함께 용출되었다는 점에서 다른 계열과 명확히 구분된다. 이는 FePO4 구조가 기본적으로 안정적임에도 표면, 입계(grain boundary) 또는 미세결함 영역에서 Fe–O–P 결합이 교환 반응에 부분적으로 관여할 수 있음을 의미한다(Zhu et al., 2013). 특히 Fe와 P는 수계에 유입될 경우 부영양화·산화반응 촉진·금속-유기복합체 형성 등 이차 생지화학적 영향을 유발할 수 있어 관리적 고려가 필요하다(Buffle, 1988; Carpenter, 2005; Gledhill and Buck, 2012).
탄산염성 분획에서 NCM811은 Ni가 가장 높은 비율을 차지하였으며 Co와 Mn도 함께 용출되었다(Fig. 3b). 이는 고함량의 Ni가 표면 수산화막 및 탄산염화 반응을 촉진하여 pH 변화에 취약한 구조를 형성하기 때문으로 여겨진다. 반면 NCM622에서는 상대적으로 높은 Mn 용출과 낮은 Ni와 Co 용출 특성을 보였다. 이에 반해 NCM523은 Ni, Co, Mn이 일정한 비율로 용출되었다. 이는 고함량의 Ni를 가진 양극재 내 잉여의 Ni가 불안정한 결합상태로 존재하며, 저함량 Ni를 가진 양극재에서는 상대적으로 강한 결합상태로 존재하는 Ni보다는 결합상태가 약한 전이금속류가 먼저 용출되는 것을 지시하며, 탄산염성 분획에서 전이금속 용출특성은 Ni 지배형(NCM811) → Mn-Li 혼합형(NCM622) → 균등 용출형(NCM523)으로 구분될 수 있음을 나타낸다. LFP에서는 Fe와 P의 용출 특성을 보였으며, 이는 인산염 기반 구조에서 H+과의 반응에 의해 Fe–P–O 결합 일부가 영향을 받는 것을 지시한다. 전이금속 독성 측면에서 Fe는 위험성이 낮지만(Boyd and Shanas, 1963), P의 용출은 하천·호수 부영양화의 직접적 공급원이 될 수 있다(Comber et al., 2013). 따라서 LFP는 환경 내에서 산성화에 의해 Fe와 P 방출이 발생해 심각한 환경 변화를 초래할 수 있을 것으로 예상된다.
산화물성 분획에서 NCM계열 모두에서 Ni, Co, Mn 용출이 나타났으며, Ni 함량이 가장 큰 NCM811에서 모든 전이금속의 농도가 가장 컸다(Fig. 3c). 이는 표면에 흡착·공침된 잉여의 전이금속 혹은 환원에 의한 전화불균형을 맞추기 위해 약한 결합상태의 전이금속이 용출된 결과로 판단된다(Stone, 1990). LCO에서는 이온교환성과 탄산염성 분획과는 달리 높은 Co 용출을 보였다(Fig. 3c). 이는 Li는 대부분 격자 내부에 고정되어 있으나, Co는 Fe–Mn 산화물과 계면 형태로 존재해 산화-환원 변화에 쉽게 용출될 수 있음을 의미한다(Ramanujapuram et al., 2016). 따라서 LFP는 일반적 자연환경에서는 상대적으로 안정적이지만 산화환원환경에서는 심각한 Co 용출이 발생할 가능성이 높다. LFP의 산화물성 분획에서는 가장 큰 P의 용출이 나타났으며, 이는 환원과정 중 인산염의 해리가 발생함에 기인한 것으로 판단된다. 따라서 LFP는 독성 전이금속보다는 영양염 기반 환경 영향 측면에서 관리가 요구되는 소재로 평가된다.
환경적 의미
현재 전 세계적으로 사용 후 LIB의 재활용률은 여전히 낮은 수준에 머무르고 있으며, 소형 전자기기(스마트폰, 노트북, 보조배터리 등)에 사용된 상당량의 LIB가 폐전자제품(e-waste)과 함께 일반 매립지로 유입되는 것으로 보고되었다(Roy et al., 2021). 이러한 처리 실태는 LIB 사용량이 급격히 증가하는 현 상황을 고려할 때, 향후 대량의 폐 LIB에 의한 Li 및 전이금속이 토양 및 매립지 환경에 점진적으로 농축될 가능성을 시사하며, 장기적으로는 지하수 오염과 같은 환경 문제로 이어질 수 있다(Beinabaj et al., 2023; Du and Li, 2023). 이번 연속추출 결과는 폐LIB가 환경에 유입될 경우 단기·중기·장기 시간 규모에 따라 Li 및 전이금속의 이동 경로가 단계적으로 확산될 수 있음을 보여준다. 다수의 양극재(NCM523, NCM622, LCO, LFP)는 장기적으로 제한적인 용출 거동을 보인 반면, Ni가 가장 부화된 NCM811은 시간 경과에 따라 지속적인 Li 해리가 진행되어 상대적으로 높은 누적 용출 가능성을 보였다. 이는 LIB내 Li가 단일 환경 조건에서 일시적으로 방출되는 것이 아니라 환경 내 pH 및 산화·환원 환경 변화에 따라 순차적으로 용출될 수 있음을 지시하며, 이러한 특성은 폐LIB가 장기적으로 다중 환경오염 위험을 내포한 잠재적 오염원으로 작용할 수 있음을 시사한다.
한편 폐LIB가 매립된 매립지는 환경적 리스크와 더불어 잠재적인 자원 저장소로서의 이중적 성격을 지닌다(Lv et al., 2018). 세계적 금속 수요 증가와 원료 확보 경쟁이 심화되는 상황에서 매립된 양극재에 농축된 Li, Ni, Co, Mn 및 일부 P은 추가적인 채굴 없이 회수가 가능한 도시광산 자원으로 활용될 잠재력을 가진다(Harper et al., 2019). 따라서 향후 폐LIB 관리는 환경 오염을 최소화하기 위한 선제적 차단 전략과 동시에 자원 회수 가능성을 고려한 순환자원화 관점이 병행된 통합 관리 체계로 전환될 필요가 있다.
결 론
이번 연구에서는 양극재에 대한 연속 추출법을 통하여 분획별 Li 및 전이금속의 농도를 분석하였고, 양극재 내 각 원소의 존재형태에 따라 환경에서의 이동성과 용출 경로가 현저히 구분된다는 점을 확인하였다. 특히 NCM811은 모든 분획에서 유사한 Li 용출 함량을 보였으며, 전이금속류 중 Ni, Co, Mn 역시 분획별 환경 변화에 따라 순차적 용출 가능성이 확인되었다. 이는 폐LIB가 수계 환경으로 유입될 경우 상대적으로 높은 이동성과 독성 금속 동시 방출로 인해 잠재적 환경 위해성을 유발할 수 있는 고위험군 소재임을 시사한다. 반면 LCO는 이온교환성과 산화물성 분획에서는 안정적인 거동을 보였으나, 장기간 산화-환원 조건이 반복되는 지하수 및 매립지 환경에서는 Co가 선택적으로 용출되어 시간 누적 따른 환경 위해성 증가 가능성이 존재하는 것으로 보였다. 이는 LCO가 단기적 관점에서는 안정적인 금속 저장 구조를 가지는 반면, 지화학적 조건 변화가 반복될 경우 Co 용출로 인한 장기적 환경 위험을 내포하는 소재임을 의미한다. LFP는 이온교환성 분획에서는 전이금속 용출이 거의 관찰되지 않아 구조적으로 안정적인 양극재로 평가되었으나, 산화·환원 및 pH 변화가 반복되는 장기적 시간규모의 환경에서는 P의 지속적 용출로 인해 부영양화, 미생물 활성 변화, Fe–P 침전–재용출 과정을 통한 생지화학적 교란 가능성을 보였다. 이러한 결과는 LFP가 중금속 독성 측면에서는 비교적 안전하다는 기존 인식과 달리, 장기적인 환경 영향의 유형이 상이하게 나타날 수 있음을 시사한다.